24.06.2009
TENTÜRDİYOT Solüsyon
İyot 2 %, Sodyum iyodür 2.5 %
Piyasa Şekilleri:
20 ml, 50 ml, 1000 ml'lik şişelerde.
Kullanım Şekli:
Yara ve sıyrıkların tedavisinde dezenfeksiyon amacıyla günde 2-3 defa bir parça pamukla sürülerek kullanılır.
Endikasyonları:
Antiseptik ve dezenfektan etkilidir. Cerrahi el dezenfeksiyonu, cilt ve yara dezenfeksiyonu, operasyon sahasının hazırlanması, yara tedavisi, mukoza dezenfeksiyonu ve yanık tedavisinde endikedir.
Kontrendikasyonları:
Nontoksik nodüler guatrda ve aşırı iyot duyarlığı bulunan kişilerde kontrendikedir.
Uyarılar:
Göze değdirilmemelidir. Kazaya uğramış derinin büyük ölçüdeki yüzeyi üzerinde kullanılmaktan sakınılmalıdır. Çünkü iyodun aşırı bir absorpsiyonu olabilir. Tiroid hastaları, yeni doğanlar, süt çocukları ve gebelerde dikkatli olunmalı ve uzun süre kullanılmamalıdır.
Yan Etkileri:
İyoda karşı duyarlı olan kişilerde alerjik reaksiyonlar görülebilir.
İlaç Etkileşimleri:
Tiroid fonksiyon testlerini bozabilir.
AIDS Hakkında
HIV vücuda girdiğinden itibaren, vücutta bununla savaşmak için özel antikorlar oluşur. Kandaki bu antikorların ELISA yöntemiyle saptanmasına Anti-HIV testi denir. HIV antikorlarının ELISA yöntemiyle ölçülebilecek düzeye ulaşması için 3 aylık bir süreye (pencere dönemi) ihtiyaç vardır. Bu nedenle test, bulaşma olduktan 3 ay sonra yapılmalıdır.
Anti-HIV testinin pozitif (seropozitif) olduğunu söyleyebilmemiz için Western Blot testi denen doğrulama testininde yapılıp sonucunun pozitif olması gerekmektedir. Anti-HIV testi, üniversite hastanelerinin mikrobiyoloji laboratuvarlarında, sigorta ve devlet hastanelerinde ve özel laboratuvarlarda yaptırılabilir.
AIDS hakkında doğru sanılan yanlışlar:
İlk olarak eşcinsellerde ortaya çıkan AIDS hastalığı konusunda vatandaşlar arasında kabul edilen anlayışların pek çoğu gerçekleri yansıtmıyor.
- AIDS, kişilerarası normal temaslarla, kapı kollarından, havlulardan, paradan, sabundan bulaşmaz. �AIDS ter, idrar ve dışkı ile yayılır ve bulaşır� kavramları yanlıştır. Sivrisinekler, AIDS bulaştırmaz.
Sağlık Bakanlığı�ndan alınan bilgiye göre, birçok kişi halen, bu hastalığı �homoseksüel� hastalığı olarak bildiği için test yaptırmaktan kaçınıyor. Vatandaşlar arasında hastalıkla ilgili genellikle yanlış bilgiler, söylenti şeklinde kulaktan kulağa yayılıyor ve bunlara zamanla inanılıyor.
Bilim adamları, AIDS konusunda bilinmesi gerekenleri şöyle sıralıyor:
Sadece cinsel ilişki ve kan yoluyla geçen AIDS, yalnızca homoseksüel hastalığı değil. Karşı cins ile ilişki de belirgin geçiş yollarından biri.
AIDS, kişilerarası normal temaslarla, kapı kollarından, yatak çarşaflarından, havlulardan, paradan, sabundan, ortak kullanılan banyo, sauna, kaplıcalar ve plajlardan bulaşmaz.
�AIDS ter, idrar ve dışkı ile yayılır ve bulaşır� kavramları yanlış.
Sivrisinekler, AIDS bulaştırmaz.
AIDS virüsü taşıyan bir kimsenin kullandığı iğnenin, herhangi bir nedenle paylaşılması virüsü bulaştırır.
Cinsel ilişki sırasında doğru prezervatif kullanımı, AIDS�in bulaşmasını önler.
Gebelikte AIDS virüsü taşıyan bir anneden, bebeğine virüs bulaşması olasılığı vardır.
AIDS virüsünü taşıyan kişiyi, hastalık belirtileri çıkmadan sağlıklı kişilerden ayırt etmek için test yapılmalıdır.
Türkiye'de AIDS:
Sağlık Bakanlığı Temel Sağlık Hizmetleri Genel Müdürlüğü Bulaşıcı Hastalıkların Kontrolü Daire Başkanlığı Zührevi Hastalıklar Şubesinin verilerine göre, en fazla vaka ve taşıyıcı 30-34 arası yaş grubunda bulunurken, bulaşma yollarının başında heteroseksüel cinsel ilişki geliyor.
En fazla hasta ve taşıyıcı, sırasıyla İstanbul, İzmir ve Ankara�da yaşıyor. İstanbul�da 181�i hasta, 551�i taşıyıcı olmak üzere toplam 732, İzmir�de 53�ü hasta, 157�si taşıyıcı olmak üzere toplam 210, Ankara�da ise 41�i hasta, 84�ü taşıyıcı olmak üzere toplam 125 aids vakası bulunuyor.
Türkiye�de bildirilen AIDS vaka ve taşıyıcılarının yıllara göre dağılımı şöyle:
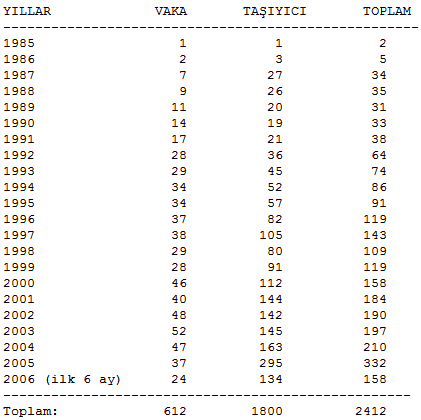 |
YAŞ GRUPLARI VE CİNSİYETE GÖRE DAĞILIM
Türkiye�deki AIDS vakalarının yaş grupları ve cinsiyete göre dağılımı da şöyle:
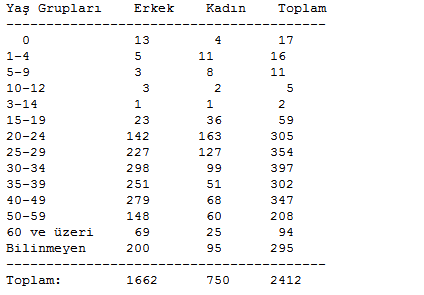 |
BULAŞMA YOLLARI
Bulaşma yollarına göre AIDS vaka ve taşıyıcılarının dağılımı ise şöyle:
 |
İLLERE GÖRE DAĞILIM
Sağlık Bakanlığı verilerine göre AIDS hastası ve taşıyıcıların bildirim yapılan ilk 10 ile göre dağılımı şöyle:
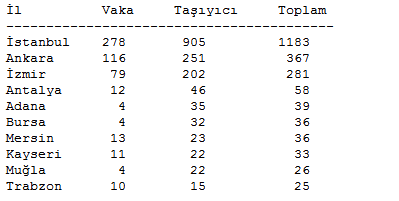 |
En fazla AIDS vaka ve taşıyıcısının yaşadığı ilk 10 il ise şöyle:
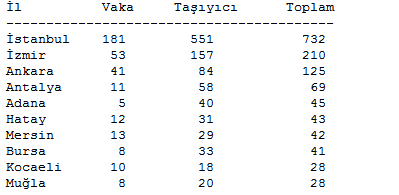
AIDS'in Belirtileri:
AIDS ve aynı virüs tarafından meydana getirilen diğer hastalıkların belirtileri hemen hemen aynıdır. Aynı soğuk ve gribin birbirleriyle özdeşleştirlmesi gibi.Fakat AIDS'e ya da ilgili hastalıklarından birine yakalanmış bir kişi için bu belirtiler çok ısrarcıdır ve nedeni yok gibi görünür. Kişi hiçbir zaman kendisini neyin hasta ettiğini bulamaz ve hastalığın üstesinden gelemez. Çünkü sadece doktorlar ve konu ile ilgili araştırma yapan bilim adamları bu belirtileri teşhis edebilirler. Bu belirtilerin doktor tarafından açıklanan bir kısmı şöyledir:
- Fiziksel ve zihinsel aktiviteleri etkileyen, sebebi açıklanamayan aşırı bir yorgunluk
- Zayıflama yada diyet gibi herhangi bir aktivite söz konusu olmadan iki aydan kısa bir sürede 7-10 kilo kaybı
- Birkaç haftanın sonunda ateşin açıklanamayacak bir şekilde 39 derecenin üstüne çıkması
- Uyku sırasında kişinin üstünü sırılsıklam edecek derecede terleme
- Sebebi bilinmeyen bir şekilde vücuttaki salgı bezlerinin kabarması (Özellikle boğazda, boyunda ve koltuk altında bulunan lenf bezlerinin kabarak en geniş halini alması)
- Dilin üzerinde ve ağız içinde beyaz noktalar yada lekelerin oluşması
- Israrla devam eden ishal
- Herhangi bir solunum enfeksiyonuyla meydana gelen ve çok uzun süren kuru öksürük
- Özellikle öksürükle birlikte oluşan nefes darlığı
- Deri üstünde ya da altında oluşan kat kat, yada yükselen bir şekilde leke ve şişliklerin meydana gelmesi. Başlangıçta çürükmüş gibi algılanabilir fakat bunlar zamanla kaybolmazlar ve genellikle etraflarındaki derilerden çok daha serttirler.
En Sık Sorulan Sorular:AIDS Hakkında En Çok Sorulan Sorular
AIDS'li kişiye dokunmak, el sıkışmak veya sarılmak tehlikeli mi?
Hayır. HIV, hapşırmak ve öksürmekle bulaşmaz. Köpek, kedi ve diğer hayvanlardan virüsü kapmazsınız.
Hastalığın belirtileri nelerdir?
Virüs alındıktan semptomlar başlayana kadar geçen süre genellikle iki - dört haftadır. Ateş gece terlemesi, kilo kaybı, artan öksürük, nefes darlığı, faranjit, yüzde ve gövdede döküntü, ağız ve genital bölgelerde lekeler, ishal, bulantı, kusma, yutma zorluğu, erken doygunluk hissi, mide kanaması, karın ağrısı ise virüsün tipik semptomları olarak rapor edilmiştir. Hastalığın klinik döneminde ise vücutta lenf nodlarının büyüdüğü ve yavaş ilerleyen zatürree tablosunun oluştuğu da dikkat çeker.
AIDS testi nerede yaptırılır?
Hemen hemen tüm devlet ve üniversite hastanelerinde testi yaptırabilirsiniz. Ayrıca pek çok özel hastanede ve laboratuvarda da Eliza testi yaptırıyor.
AIDS testinde neye bakılır?
HIV vücuda girdiğinden itibaren, vücutta bununla savaşmak için özel antikorlar oluşur. Eliza diye bilinen testle kanda, hastalığa sebep olan mikroba karşı gelişmiş olan antikor olup olmadığına bakılır. Antikorların Eliza yöntemiyle ölçülebilecek düzeye ulaşması için 3 aylık bir süreye (pencere dönemi) ihtiyaç vardır. Bu nedenle test, bulaşma olduktan 3 ay sonra yapılmalıdır.
Test sonucu HIV(+) (HIV Pozitif) çıkarsa kişi kanında bu antikorları taşıyor demektir. Bu da kişinin AIDS virüsüyle karşılaştığı anlamına gelir. Ancak testin yalancı pozitif çıkma ihkimali de vardır. Kişinin HIV pozitif olduğunun seylenebilmesi için Westernblood testi denen doğrulama testinin de yapılıp sonucunun pozitif olması gerekir.
Eğer test (-) çıkarsa bu, kişinin AIDS virüsü taşımadığı anlamını taşımıyor. Emin olmak için üçüncü ayın sonunda tekrar test yaptırılır. Çünkü kan testi virüs vücuda girdikten 3 ay sonrasına kadar virüsü gösteremeyebilir. Üçüncü ay yapılan test yine (-) çıkarsa rahatlayabilirsiniz.
Test olmak için isim vermek şart mı?
Kendi isminizi söylemek zorunda değilsiniz. Hiç bir özel hastane ya da laboratuvarın nüfus cüzdanınızı ya da fotokopisini isteme hakkı yok. Sağlık Bakanlığı'nın da bu konuda genelgesi bulunuyor.
Pozitif çıkarsa herkes duyar mı?
AIDS, Sağlık Bakanlığı'na bildirilmesi zorunlu bir hastalık. Bu, istatistikler yapmak, durumu ve gidişi belirlemek için gerekli. Ama bu bildirim isimle yapılmıyor. İsminizin baş harfleri ve doğum yılınız kullanılarak kodlanıyor. Bunun dışında tedavinizden sorumlu doktor ve ekibi dışında kimseye söylenmemesi gerekiyor. Tüm tedavi masrafları her sigorta kuruluşu tarafından karşılanıyor. Sigortası olmayıp, maddi gücü de yeterli olmayanlar yeşil karttan yararlanabiliyor.
Test yaptırdım HIV (+) çıktı. Bu AIDS hastası olduğum anlamına mı geliyor?
HIV (+)" test sonuçları, sizin AIDS'e neden olan virusla (HIV) enfekte olduğunuz anlamına geliyor. CD4+ T hücre sayınız 200hücre/mm3'ün altına düştüğünde ve/veya AIDS ile ilişkili bir hastalık (fırsatçı enfeksiyonlar ve Kaposi Sarkomu gibi) gelişirse HIV , AIDS hastalığına doğru ilerler.
HIV hastalarında sıkça görülen ruhsal bozukluklar nelerdir?
En sık karşılaşılanı depresyondur. Depresyon AIDS hastalarında normal popülasyondan yüzde 40 daha fazla görülür. Bunaltı bozuklukları yüzde 2 - 38 oranlarında görülmektedir. İntihar riski normal kontrollerden 10 kat daha fazladır. Depresyon, eşcinsellik ve madde kullanımı riskini arttırmaktadır. HIV pozitif olduğunu öğrendikten sonra ve yakın bir zamanda AIDS'li bir arkadaşın kaybından sonra intihar oranları artmaktadır.
HIV virüsü dış ortamda yaşayabilir mi?
HIV, açık havaya maruz kaldığında uzun süre yaşayamaz. Dış ortamda ısı, kuruma, su, sabun ve deterjanlar nedeniyle tahrip olur. Spermdeki ve vajina salgısındaki HIV, dış ortamda birkaç saatte, kuru ortamda ise yarım saatte ölür. HIV kurumuş kanda da kısa zamanda ölür. Yine de dökülmüş kan, sperm ve diğer beden sıvıları küçük de olsa risk oluşturur. Bu yüzden sulandırılmış çamaşır suyu ya da eşyanın bir kaç dakika kaynatılarak temizlenmesi gerekir.
Hamile kalırsam, bebeğime HIV virüsü bulaşır mı?
Anti-HIV ilaçları, hamile anneden bebeğine HIV geçme riskini önemli ölçüde azaltabilir. Hamileyseniz ve veya hamile kalmayı düşünüyorsanız, doktorunuza danışmanızda fayda var.
Türkiye'de kaç tedavi merkezi var?
Türkiye'de AIDS konusunda tedavi veren ilk merkez 1997 yılında Prof. Dr. Serhat Ünal başkanlığında kurulan Hacettepe AIDS ve Tedavi Merkezi (HATAM), İstanbul Tıp Fakültesi ve İzmir'de Ege Üniversitesi'nde AIDS merkezi bulunmaktadır.
Tedavi yöntemleri nelerdir?
AIDS tedavisi için ilk ilaç 1985'te çıktı. Halen bu ilaç kombinasyonu kullanılıyor. Kesin tedavi söz konusu değil ancak ilaç alındığı sürece hasta normal yaşam süresinde yaşayabiliyor. Yaşam boyu düzenli olarak kullanılması gerekiyor. İlacın yan etkileri olduğu gibi hastalığın ilerleme seviyesine göre ilacın etkisi de olmayabiliyor.
Tedavide son durum nedir?
Dünyanın en büyük ilaç firmalarından Merck Sharp & Dohme İlaçları, üzerinde çalıştığı AIDS aşısının gelecekte hastalığa çözüm sağlayacağını açıkladı. Maymunlar üzerinde oldukça iyi sonuçlar veren aşının insan üzerinde de denendi. Yeni AIDS aşı için uzmanlar aşının daha çok vücudun bağışıklık sistemini güçlendirerek virüsün kontrol altında tutulmasını sağlayacağını veya uzun yıllar hastalığın başlamasına engel olacağını ümit ediyorlar. Her şeyin mükemmel gitmesi halinde aşının beş yıl içinde kullanılmaya başlayacağı tahmin ediliyor.
HIV tedavisi görürken virüsü başkasına bulaştırırmıyım?
Anti-HIV ilaçları, virüsü başkalarına bulaştırmanızı önlemez. Tedavi, virüs miktarını algılanamayacak kadar düşük seviyelerde tutar. Ancak, HIV vücudunuzda varlığını devam ettirir ve cinsel ilişki, iğne paylaşımı veya annelerin bebeklerini emzirmesi yoluyla başkalarına bulaşabilir.
İyi hissediyorum, anti-HIV ilaçları almama gerek var mı?
Vücudunuzda HIV hastalığının herhangi bir belirtisi ortaya çıkmasa bile, virüs yavaş yavaş bağışıklık sisteminizi zayıflatıyor olabilir. Virüs seviyenizi ve T-hücresi sayımınızı ölçmek, durumunuz hakkında bilgi verebilir. Doktorunuzla seçeneklerinizi incelemek ve tedaviye ne zaman başlanacağını, hangi ilaçları kullanmanız gerektiğini değerlendirmek önemli.
CD4+ T hücre sayısı ne demek?
CD4+ T hücre sayısı kişinin ölçülen CD4+ T hücre miktarı demektir. HIV kişinin bu hücrelerini enfekte eder ve çoğalmak (kendi kopyasını yapar) için bu hücreleri kullanır. Bu hücreler zarar gördükçe kişinin bağışıklık sistemi zayıflar ve kişi fırsatçı enfeksiyonlara (bakteriyel, viral, parazit ve mantar gibi) daha çabuk yakalanır.
Viral Yük Nedir?
Viral yük insanın kanında bulunan virus (HIV) miktarıdır. Yüksek miktarda viral yükü olan olan kişi, düşük viral yükü olan kişiden daha çabuk AIDS geliştirir.
CD4+ T Hücresi Nedir?
CD4+T hücrelerine, akyuvarlar, T yardımcı hücreleri de denilmektedir. İnsan bağışıklık sisteminde diğer hücrelerle birlikte hastalıklara karşı savaşırlar. HIV, çoğalmak için bu hücreleri kullanır. Sağlıklı bir kimsede CD4+T hücre sayısı 800-1200/mm3 kadardır.
Kaynak: http://www.aidsnedir.com
23.06.2009
VİTİLİGO
Vitiligo deriyi boyayan maddenin (pigment ) kaybı nedeniyle, cildin beyazlaşması ile seyreden bir hastalıktır. Vitiligo vücudun herhangi bir yerini tutabilir. Genellikle vücudun her iki yanı da tutulur. En sık olarak yüz, dudak, el, kol, bacak ve cinsel bölge tutulur.
KİMLER VİTİLİGOYA YAKALANIR?
Vitiligo her yüz kişiden 1-2 sini etkiler. Etkilenen kişilerin yarısı 20 yaşın altındadır ve etkilenen beş hastadan birinin ailesinde bu hastalık tablosu vardır. Bu hastalık otoimmün (vücudun pigment hücrelerine antikor oluşturduğu) bir hastalıktır. Vitiligosu bulunan hastaların çoğu sağlıklı olmasına rağmen bazı hastalarda guatr hastalığı gibi otoimmün hastalıklar vardır.
DERİNİN RENGİNİ NE BELİRLER?
Derideki melanosit denen hücrelerden üretilen melanin adlı madde derimizin rengini(açık veya koyu renkli) oluşunu belirler. Melanosit denen bu hücreler ölür veya melanin salgılayamazlarsa derinin rengi giderek açılır ve sonunda tamamıyla beyazlaşır.
VİTİLİGO NASIL GELİŞİR?
Tipik olarak vitiligolu deri bölgesi süt beyazı renktedir. Bununla birlikte pigment kaybının derecesine göre renk değişebilir. Lekelerin içinde farklı renk tonları bulunabilir ve etrafı daha koyu bir sınırla çevrili olabilir.
Vitiligo genellikle hızlı bir pigment kaybı ile başlar. Bu süreç bilinmeyen bir nedenle pigment kaybının durmasına kadar sürer.
Hastalığın seyri ve şiddeti kişiden kişiye değişir. Açık tenli kişilerde hastalık genellikle yazın deri bronzlaşınca ortaya çıkar. Esmerlerde ise hastalık daha belirgindir. Bazı hastalarda derinin tamamı beyazlaşır.Şiddetli olgularda pigment kaybı tüm vücudu kaplar. Pigment kaybının ne kadar olacağını belirleyen bir bulgu yoktur.
VİTİLİGO NASIL TEDAVİ EDİLİR?
Bazen en iyi tedavi hastaya herhangi bir tedavi uygulamamaktır. Özellikle açık tenli olan kişilerin sadece güneşten koruyucu kremleri kullanması bile yeterli olabilir. Derinin hastalıklı alanları güneş ışınlarına karşı korumasızdır. Bu alanlarda kolaylıkla güneş yanığı gelişebilir. Koruma amacıyla en az 30 faktörlü güneşten koruyucular kullanılmalıdır.
Vitiligo lekeleri çeşitli makyaj malzemeleri, kendiliğinden bronzlaşma sağlayan kremler ile kamufle edilebilir. Bu yöntemlerle hastalık tedavi edilmez, fakat lekelerin görünümü düzeltilir. Küçük alanlara iğnelerle deri rengini verecek maddeler enjekte edilebilir. Bu yöntem özellikle küçük alanlarda etkili bir yöntemdir.
Eğer güneşten koruyucular ve kamuflaj yöntemleri etkisiz kalırsa diğer tedavi yöntemleri uygulanabilir.Tedavide yeniden normal bir pigmentasyon sağlanması amaçlanır. Bu yöntemlerin hiç birisi kalıcı çözüm vermez.
ÇOCUKLARDA VİTİLİGONUN TEDAVİSİ
Çocuklarda genellikle agresif tedaviler uygulanmaz. Güneşten koruyucular veya kamuflaj en iyi tedavi yöntemidir. Lokal kortikosteroidler dikkatli gözlem altında kullanılabilir. PUVA tedavisi 12 yaşın altında tavsiye edilmez ve bu tedaviye başlamadan evvel riskleri ve faydaları dikkatli bir şekilde değerlendirilmelidir.
PUVA -PUVA denen bir tedavi yönteminde hastaya psorelen içeren bir hap verilir. Psorelen deriyi ışığa hassas hale getirir. Daha sonra hasta morötesi ışığın bir tipi olan ultraviyole A ışığına maruz bırakılır. Bu tedavi için özel ekipman gerekir. Yüz, üst kol, üst bacak, gövde gibi alanlarda % 50-70 oranında iyileşme olur. Eller ve ayaklar ise tedaviye kötü cevap verir. PUVA tedavisi Dermatoloji Uzmanının gözetiminde yapılmalıdır. Güneş yanığına benzer şikayetler görülebilir. Uzun vadede deride çillenmeye ve cilt kanseri riskinin artmasına neden olabilir. UVA göze de zararlı olduğundan UVA filtresi olan gözlükler seans sırasında ve dışarı güneşe çıkıldığında kullanılmalıdır. Bu gözlüklerin kullanımı katarak gelişimini engeller. 12 yaşın altında, hamilelerde ve bebek emziren kadınlarda PUVA tedavisi uygulanamaz.
Dar bant UVB - Bu tedavi şeklinde haftada 2-3 seans bir kaç ay boyunca tedaviye alınır Bu tedavinin şu an geniş kullanımı yoktur. Butedavi yöntemi özellikle çocuk hastaları tedavi etmekte kullanılabilir.
Grafting - Normal sağlıklı derinin sağlıksız alana cerrahi yollarla aktarılması (grafting) az sayıda hastada faydalı olabilen bir yöntemdir. Ayrıca hastalıklı alanın tamamında homojen bir renk dönüşü olmaz.
DİĞER TEDAVİ YÖNTEMLERİ
Diğer tedavi şekilleri arasında, bağışıklık sistemini düzenleyen maddeler içeren kremlerin kullanımı vardır. Güvenli olduğundan çocuklara ve göz kapağına da uygulanabilir. Excimer laser de tedavi de denenebilir.
VİTİLİGO KESİN OLARAK TEDAVİ EDİLEBİLİR Mİ?
Günümüzde vitiligonun nedeni bilinmemektedir, bununla beraber hastalığın ailesel bir özelliği vardır. Hastalığı tedavi edecek çeşitli yöntemler bulunmasına rağmen, hastalığın kesin bir tedavisi yoktur. Vitiligo ile ilgili yapılan araştırmalar halen sürmektedir.
EXELON Oral Solüsyon
Rivastigmin 2 mg/ml
Piyasa Şekilleri:
120 ml'lik şişelerde ve doz şırıngası ile.
Kullanım Şekli:
Rivastigmin sabah ve akşam yemeklerinde olmak üzere günde 2 defa alınmalı; kapsüller bir bütün olarak, çiğnenmeden yutulmalıdır. Başlangıç dozu: Günde 2 defa 1.5 mg. Önerilen başlangıç dozu, günde 2 defa 1.5 mg'dır. Bu doz, en az 2 hafta devam eden bir tedaviden sonra, iyi tolere edilirse doz günde 2 defa 3 mg'a yükseltilebilir. Dozun daha sonra günde 2 defa 4.5 ve 6 mg'a yükseltilmesi, her bir dozla minimum 2 haftalık tedavi sonrasında ve hastanın o dozu iyi tolere etmesinden sonra düşünülmelidir. İdame dozu: Günde 2 defa 3-6 mg'dır. Önerilen maksimal günlük doz, iki defa 6 mg'dır. İdame tedavisi, hasta terapötik fayda görmeye devam ettiği sürece uygulanmalıdır. Terapötik etki kanıtları ortadan kalkarsa, tedaviye son verilmesi düşünülmelidir. 6 aydan daha uzun süren çalışmalarda incelenmiş değildir. Tedaviye birkaç günden daha uzun süre ara verilmişse, günde 2 defa 1.5 mg rivastigminle tekrar başlatılmalıdır. Rivastigmin maruz kalımının böbrek bozukluğunda, ayrıca hafif-orta şiddetteki karaciğer bozukluğunda artmış olması nedeniyle; bireysel tolerabiliteye göre gerçekleştirilecek dozaj titrasyonu önerilerine yakından uyulmalıdır.
Endikasyonları:
Alzheimer hastalığındaki veya Parkinson hastalığına eşlik eden hafif-orta şiddetteki demansın semptomatik tedavisi.
Kontrendikasyonları:
Rivastigmine, diğer karbamat türevlerine veya formülasyonun diğer bileşenlerine karşı bilinen aşırı duyarlığı olan hastalarda ve şiddetli karaciğer bozukluğu olan hasta popülasyonunda incelenmemiş olduğundan kontrendikedir.
Uyarılar:
Sinüs sendromu veya şiddetli kardiyak aritmi vakalarında diğer kolinomimetiklerde olduğu gibi, rvastigmin kullanırken de dikkatli olmak gerekir. Kolinerjik uyarı, mide asidi salgısının artmasına neden olabilir. Daha önce solunum hastalığı geçirmiş olan veya tedavi sırasında solunum hastalığı bulunan vakalar da dahil olmak üzere, rivastigmin ile tedavi edilen hastalarda solunum sistemiyle ilgili yeni belirtiler ve semptomlar gelişmemiş, ya da mevcut belirti ve semptomlar şiddetlenmemiştir. Ancak diğer kolinomimetikler gibi rivastigmin de bu hastalarda dikkatle kullanılmalıdır. Akut bronşiyal astım hastalarının rivastigmin ile tedavisi konusunda herhangi bir deneyim yoktur. Kolinomimetikler üriner obstrüksiyonu ve konvülsiyonları şiddetlendirebilir. Hayvanlarda yapılan çalışmalarda rivastigmin herhangi bir teratojen etki göstermemiştir. Ancak gebe kadınlardaki ilaç emniyeti saptanmış değildir ve gebe kadınlarda bu ilaç ancak, beklenen faydalar, fetusun görebileceği zararlardan fazla olduğu takdirde kullanılmalıdır. anne sütüne geçip geçmediği bilinmediğinden, bu ilacı kullanan anneler bebeklerini emzirmemelidir. Tedavi edilen hastalarda herhangi bir hareket fonksiyonu bozukluğu görülmemiştir. Ancak Alzheimer hastalarının araç veya karmaşık makineleri kullanmaya devam etme konusundaki yetenekleri, kendilerini tedavi eden doktor tarafından rutin olarak değerlendirilmelidir.
Yan Etkileri:
Advers etkilerin sıklık ve şiddeti genellikle yüksek dozlarda artmaktadır. Genel bozukluklar: Yorgunluk, güçsüzlük. Santral ve periferik sistem bozuklukları: Baş dönmesi, baş ağrısı, uyku hali. Gastrointestinal sistem bozuklukları: Bulantı, kusma, diyare, karın ağrısı, iştah kaybı, dispepsi. Kadın hastaların bulantı, kusma, iştah kaybı ve kilo kaybı gibi advers etkilere daha duyarlı oldukları bulunmuştur.
İlaç Etkileşimleri:
Rivastigmin, başlıca esterazlar tarafından hidroliz yoluyla metabolize edilir. Sitokrom P450 izoenzimleri tarafından minimal bir metabolizma söz konusu olduğundan rivastigminin, bu enzimlerin metabolize ettiği diğer ilaçlarla herhangi bir farmakokinetik etkileşim göstermesi beklenmez. Farmakodinamik etkileri göz önünde tutularak, diğer kolinomimetik ilaçlarla birlikte verilmemelidir, antikolinerjik ilaçların etkisini bozabilir. Bir kolinesteraz inhibitörü olarak rivastigmin, anestezi sırasında süksinilkolin-tipi kas gevşeticilerin etkilerini şiddetlendirebilir.
BEVİTOL Tablet
Vitamin B1 (Tiamin) 250 mg, Vitamin B6 (Piridoksin) 250 mg
Kullanım Şekli:
Günlük tedavi dozu 2-4, profilaktik dozu 1-2 tablettir.
Endikasyonları:
Nevrit, polinevrit, diyabetik nöropati, gebelik nevriti, artrit, periartrit, siyatik, lombalji, artralji, miyalji, kramp, romatizma ağrıları, idiyopatik ve ihtiyarlığa bağlı tremor, Wemicke hastalığı, Korsakoff psikozu, delirium tremens, gebelik, radyoterapi, iştahsızlık, bulantı ve kusmalarda endikedir.
Kontrendikasyonları:
Bileşimdeki vitaminlerden herhangi birine karşı aşırı duyarlılığı olanlarda kullanılmamalıdır.
Uyarılar:
Bileşimdeki piridoksin levodopanın periferik metabolizmasını artırdığından tek başına levodopa müstahzarı kullanan parkinson hastalarına verilmemelidir.
Yan Etkileri:
Herhangi bir yan etkisi olmamasına rağmen çok yüksek dozlarda kullanılmaması gerektiği gözönünde bulundurulmalı ve B grubu vitaminlere duyarlı kişilere verilmemelidir.
İlaç Etkileşimleri:
B6 vitamini levodopanın etkisini antagonize edebileceğinden parkinson tedavisinde sadece levodopa alanlara verilmez. Levodopa+benserazid kombinasyonu alanlarda kullanılabilir.
22.06.2009
EMEDUR Supozituvar
Trimetobenzamid HCl, Benzokain
Piyasa Şekilleri:
100 mg, 20 mg: 5 supozituvar, 200 mg, 40 mg: 5 supozituvar içeren ambalajlarda.
Kullanım Şekli:
15 kg'ın altındaki çocuklarda günde 3-4 kez 100 mg'lık 1 supozituvar; 15-45 kg arası çocuklarda günde 3-4 kez 100 mg'lık 1 supozituvar veya 2 adet 200 mg'lık supozituvar uygulanır.
Endikasyonları:
Bulantı ve kusmanın kontrolünde kullanılır.
Kontrendikasyonları:
Trimetobenzamide ve müstahzarların supozituvar formlarının içerdiği benzokaine karşı aşırı duyarlılığı olanlarda kontrendikedir.
Uyarılar:
Akut ateşli hastalıklar, ensefalitiler, gastroenterit, dehidratasyon ve elektrolit dengesizliği halinde trimetobenzamid ve diğer antiemetiklerle veya antiemetik kullanmaksızın özellikle çocuklar, yaşlılar ve zayıf kişilerde SSS reaksiyonları (örn. opistotonus, konvülziyonlar, koma ve ekstrapiramidal semptomlar) bildirilmiştir. Bu gibi durumlarda özellikle yakın geçmişte fenotiyazin türevleri, barbitürat ve belladon türevi gibi SSS'ni deprese eden ajanları kullananlarda trimetobenzamid ihtiyatla kullanılmalıdır. Şiddetli kusmalarda yalnızca antiemetik verilmemeli, kusmanın nedeni belirlenmelidir. Herşeyden önce kaybolan vücut sıvısınının yeniden sağlanması, elektrolit dengesinin düzeltilmesi, ateşin düşürülmesi ve kusma nedeninin ortadan kaldırılması üzerinde durulmalıdır. Aşırı hidratasyondan kaçınılmalıdır, çünkü serebral ödem oluşabilir. Trimetobenzamidin antiemetik etkisi apandisit gibi olguların teşhisini veya diğer ilaçların doz aşımına bağlı toksik belirtilerinin anlaşılmasını güçleştirebilir. Çocukların kusmalarında trimetobenzamid kullanırken tedbirli olunmalıdır, çocukların basit kusmalarında antiemetikler verilmemelidir, yalnızca nedeni bilinen kusmalarda kullanılmalıdır, çünkü santral sinir sistemine etki eden antiemetiklerin virüs enfeksiyonlarıyla birleştiğinde REYE sendromunun gelişmesine neden olabileceği düşünülmektedir. REYE sendromu çocuklarda, ölümle sonuçlanabilen akut ensefalopatidir. Bu kuşkuyu doğrulayan herhangi bir bulgu olmadığı halde tedbirli olunması önerilir. Trimetobenzamide bağlı olarak ortaya çıkabilecek ekstrapiramidal semptomlar, kusmaya neden olan teşhis edilmiş hastalığın, örneğin REYE sendromu veya diğer ensefalopatilerin SSS belirtileriyle karışabilir. Trimetobenzamid uyku hali oluşturabilir. Bu nedenle hastanın ilaca kişisel tepkisi anlaşılıncaya kadar motorlu araç ve tehlikeli makineleri kullanmamaları önerilir. Trimetobenzamid alkolle birlikte kullanılmamalıdır. Trimetobenzamidle yapılan çalışmalarda, sıçan ve tavşanlarda teratojenik etki görülmemiştir. Gebelerde ve emziren annelerde yeterli çalışmalar yapılmadığı için güvenilirliği yeterince kanıtlanmamıştır. Bu nedenle gebelerde, emziren annelerde kullanılması sakıncalı olabilir.
Yan Etkileri:
Aşırı duyarlılık reaksiyonları ve parkinson benzeri semptomlar bildirilmiştir. Kan diskrazileri, görme bulanıklığı, konvülziyon, diyare, depresyon, baş dönmesi, baş ağrısı, uyuşukluk, sarılık, kas krampları ve opistotonus bildirilmiştir. Bunlardan herhangi biri görüldüğünde ilacın kullanımına son verilmelidir. Alerjik tipte deri reaksiyonları görülmüştür. İlk duyarlılık belirtisinde ilacın kullanımı hemen durdurulmalıdır. Belirtiler zamanla kaybolabildiği gibi bazı olgularda semptomatik tedavi gerekebilir.
İlaç Etkileşimleri:
Trimetobenzamid trisiklik antidepresanlar, SSS'ne etkili antihipertansifler, SSS depresanları, parenteral magnezyum sülfatla etkileşebilir, trimetobenzamidin veya bu ilaçların etkileri artabilir. Trimetobenzamid sisplatin, paromomisin, salisilatlar ve vankomisin gibi ototoksik ilaçların kulak çınlaması ve baş dönmesi gibi belirtilerini maskeleyebilir.
EMEDUR Draje
Trimetobenzamid HCl 200 mg
Piyasa Şekilleri:
20 drajelik ambalajlarda.
Kullanım Şekli:
Ortalama yetişkin dozu günde 3-5 kez 1 drajedir. 15-45 kg arası çocuklarda günde 1-4 kez 1 draje verilir.
Endikasyonları:
Bulantı ve kusmanın kontrolünde kullanılır.
Kontrendikasyonları:
Trimetobenzamide ve müstahzarların supozituvar formlarının içerdiği benzokaine karşı aşırı duyarlılığı olanlarda kontrendikedir.
Uyarılar:
Akut ateşli hastalıklar, ensefalitiler, gastroenterit, dehidratasyon ve elektrolit dengesizliği halinde trimetobenzamid ve diğer antiemetiklerle veya antiemetik kullanmaksızın özellikle çocuklar, yaşlılar ve zayıf kişilerde SSS reaksiyonları (örn. opistotonus, konvülziyonlar, koma ve ekstrapiramidal semptomlar) bildirilmiştir. Bu gibi durumlarda özellikle yakın geçmişte fenotiyazin türevleri, barbitürat ve belladon türevi gibi SSS'ni deprese eden ajanları kullananlarda trimetobenzamid ihtiyatla kullanılmalıdır. Şiddetli kusmalarda yalnızca antiemetik verilmemeli, kusmanın nedeni belirlenmelidir. Herşeyden önce kaybolan vücut sıvısınının yeniden sağlanması, elektrolit dengesinin düzeltilmesi, ateşin düşürülmesi ve kusma nedeninin ortadan kaldırılması üzerinde durulmalıdır. Aşırı hidratasyondan kaçınılmalıdır, çünkü serebral ödem oluşabilir. Trimetobenzamidin antiemetik etkisi apandisit gibi olguların teşhisini veya diğer ilaçların doz aşımına bağlı toksik belirtilerinin anlaşılmasını güçleştirebilir. Çocukların kusmalarında trimetobenzamid kullanırken tedbirli olunmalıdır, çocukların basit kusmalarında antiemetikler verilmemelidir, yalnızca nedeni bilinen kusmalarda kullanılmalıdır, çünkü santral sinir sistemine etki eden antiemetiklerin virüs enfeksiyonlarıyla birleştiğinde REYE sendromunun gelişmesine neden olabileceği düşünülmektedir. REYE sendromu çocuklarda, ölümle sonuçlanabilen akut ensefalopatidir. Bu kuşkuyu doğrulayan herhangi bir bulgu olmadığı halde tedbirli olunması önerilir. Trimetobenzamide bağlı olarak ortaya çıkabilecek ekstrapiramidal semptomlar, kusmaya neden olan teşhis edilmiş hastalığın, örneğin REYE sendromu veya diğer ensefalopatilerin SSS belirtileriyle karışabilir. Trimetobenzamid uyku hali oluşturabilir. Bu nedenle hastanın ilaca kişisel tepkisi anlaşılıncaya kadar motorlu araç ve tehlikeli makineleri kullanmamaları önerilir. Trimetobenzamid alkolle birlikte kullanılmamalıdır. Trimetobenzamidle yapılan çalışmalarda, sıçan ve tavşanlarda teratojenik etki görülmemiştir. Gebelerde ve emziren annelerde yeterli çalışmalar yapılmadığı için güvenilirliği yeterince kanıtlanmamıştır. Bu nedenle gebelerde, emziren annelerde kullanılması sakıncalı olabilir.
Yan Etkileri:
Aşırı duyarlılık reaksiyonları ve parkinson benzeri semptomlar bildirilmiştir. Kan diskrazileri, görme bulanıklığı, konvülziyon, diyare, depresyon, baş dönmesi, baş ağrısı, uyuşukluk, sarılık, kas krampları ve opistotonus bildirilmiştir. Bunlardan herhangi biri görüldüğünde ilacın kullanımına son verilmelidir. Alerjik tipte deri reaksiyonları görülmüştür. İlk duyarlılık belirtisinde ilacın kullanımı hemen durdurulmalıdır. Belirtiler zamanla kaybolabildiği gibi bazı olgularda semptomatik tedavi gerekebilir.
İlaç Etkileşimleri:
Trimetobenzamid trisiklik antidepresanlar, SSS'ne etkili antihipertansifler, SSS depresanları, parenteral magnezyum sülfatla etkileşebilir, trimetobenzamidin veya bu ilaçların etkileri artabilir. Trimetobenzamid sisplatin, paromomisin, salisilatlar ve vankomisin gibi ototoksik ilaçların kulak çınlaması ve baş dönmesi gibi belirtilerini maskeleyebilir.
EMEDUR Ampul
Trimetobenzamid HCl 200 mg/2 ml
Piyasa Şekilleri:
2 ml'lik 6 ampul, 2 ml'lik 100 ampul içeren ambalajlarda.
Kullanım Şekli:
Ortalama yetişkin dozu günde 3-4 kez 1 ampul, gluteus bölgesinin dış üst bölümüne derin olarak yapılmalıdır. Damar içine uygulanmamalıdır.
Endikasyonları:
Bulantı ve kusmanın kontrolünde kullanılır.
Kontrendikasyonları:
Trimetobenzamide ve müstahzarların supozituvar formlarının içerdiği benzokaine karşı aşırı duyarlılığı olanlarda kontrendikedir.
Uyarılar:
Akut ateşli hastalıklar, ensefalitiler, gastroenterit, dehidratasyon ve elektrolit dengesizliği halinde trimetobenzamid ve diğer antiemetiklerle veya antiemetik kullanmaksızın özellikle çocuklar, yaşlılar ve zayıf kişilerde SSS reaksiyonları (örn. opistotonus, konvülziyonlar, koma ve ekstrapiramidal semptomlar) bildirilmiştir. Bu gibi durumlarda özellikle yakın geçmişte fenotiyazin türevleri, barbitürat ve belladon türevi gibi SSS'ni deprese eden ajanları kullananlarda trimetobenzamid ihtiyatla kullanılmalıdır. Şiddetli kusmalarda yalnızca antiemetik verilmemeli, kusmanın nedeni belirlenmelidir. Herşeyden önce kaybolan vücut sıvısınının yeniden sağlanması, elektrolit dengesinin düzeltilmesi, ateşin düşürülmesi ve kusma nedeninin ortadan kaldırılması üzerinde durulmalıdır. Aşırı hidratasyondan kaçınılmalıdır, çünkü serebral ödem oluşabilir. Trimetobenzamidin antiemetik etkisi apandisit gibi olguların teşhisini veya diğer ilaçların doz aşımına bağlı toksik belirtilerinin anlaşılmasını güçleştirebilir. Çocukların kusmalarında trimetobenzamid kullanırken tedbirli olunmalıdır, çocukların basit kusmalarında antiemetikler verilmemelidir, yalnızca nedeni bilinen kusmalarda kullanılmalıdır, çünkü santral sinir sistemine etki eden antiemetiklerin virüs enfeksiyonlarıyla birleştiğinde REYE sendromunun gelişmesine neden olabileceği düşünülmektedir. REYE sendromu çocuklarda, ölümle sonuçlanabilen akut ensefalopatidir. Bu kuşkuyu doğrulayan herhangi bir bulgu olmadığı halde tedbirli olunması önerilir. Trimetobenzamide bağlı olarak ortaya çıkabilecek ekstrapiramidal semptomlar, kusmaya neden olan teşhis edilmiş hastalığın, örneğin REYE sendromu veya diğer ensefalopatilerin SSS belirtileriyle karışabilir. Trimetobenzamid uyku hali oluşturabilir. Bu nedenle hastanın ilaca kişisel tepkisi anlaşılıncaya kadar motorlu araç ve tehlikeli makineleri kullanmamaları önerilir. Trimetobenzamid alkolle birlikte kullanılmamalıdır. Trimetobenzamidle yapılan çalışmalarda, sıçan ve tavşanlarda teratojenik etki görülmemiştir. Gebelerde ve emziren annelerde yeterli çalışmalar yapılmadığı için güvenilirliği yeterince kanıtlanmamıştır. Bu nedenle gebelerde, emziren annelerde kullanılması sakıncalı olabilir.
Yan Etkileri:
Aşırı duyarlılık reaksiyonları ve parkinson benzeri semptomlar bildirilmiştir. Kan diskrazileri, görme bulanıklığı, konvülziyon, diyare, depresyon, baş dönmesi, baş ağrısı, uyuşukluk, sarılık, kas krampları ve opistotonus bildirilmiştir. Bunlardan herhangi biri görüldüğünde ilacın kullanımına son verilmelidir. Alerjik tipte deri reaksiyonları görülmüştür. İlk duyarlılık belirtisinde ilacın kullanımı hemen durdurulmalıdır. Belirtiler zamanla kaybolabildiği gibi bazı olgularda semptomatik tedavi gerekebilir.
İlaç Etkileşimleri:
Trimetobenzamid trisiklik antidepresanlar, SSS'ne etkili antihipertansifler, SSS depresanları, parenteral magnezyum sülfatla etkileşebilir, trimetobenzamidin veya bu ilaçların etkileri artabilir. Trimetobenzamid sisplatin, paromomisin, salisilatlar ve vankomisin gibi ototoksik ilaçların kulak çınlaması ve baş dönmesi gibi belirtilerini maskeleyebilir.
VALİDOL Damla
Hidroksizin HCl 50 mg/ml
Piyasa Şekilleri:
10 ml'lik renkli damlalıklı şişelerde.
Kullanım Şekli:
Psikonöroz ile bağlantılı anksiyete semptomlarda: Yetişkinlerde; 15-60 damla günde 3-4 defa, 6 yaştan küçüklerde; 7 damla 6 saatte bir, 6 yaştan büyüklere; 7-15 damla 6 saatte bir. Ameliyat öncesi: Yetişkinlerde; 30-60 damla, çocuklarda; kilo başına 0.6 mg. Alerjik nedenlere bağlı pruritlerde: Yetişkinlerde; 15 damla günde 3-4 defa, 6 yaştan büyükler; 7-15 damla günde 3-4 defa, 6 yaştan küçükler; 7 damla günde 3-4 defa.
Endikasyonları:
Anksiyete bozukluklarının semptomatik tedavisi ve yaygın anksiyete bozukluğu; kronik ürtiker, atopik veya kontakt dermatozlarda; genel anesteziden önce ve sonra sedatif olarak endikedir.
Kontrendikasyonları:
Hidroksizine karşı aşırı duyarlılığı olanlarda ve intermittant akut porfiride kontrendikedir.
Uyarılar:
Hidroksizin konvülsiyon potansiyeli yüksek hastalarda dikkatle kullanılmalıdır. Potansiyel antikolinerjik etkileri nedeniyle dar açılı glokom, üriner retansiyon riski olan prostat hipertrofileri, paralitik ileus ve myastenia gravisi olan hastalarda dikkatle kullanılmalıdır. Allerji test sonuçlarını etkilemesini önlemek için tedavi 5 gün önceden sonlandırılmış olmalıdır. Motorlu taşıt ve dikkat isteyen araç kullananlar almamalıdır. Renal fonksiyon bozukluklarında dikkatli olunmalıdır. Fetus için yarar/zarar oranı dikkate alınarak kullanılması önerilmedikçe, hidroksizin gebelik sırasında kullanılmamalıdır. Doğum sırasında kullanılması önerilmez. Süte geçip geçmediği belli olmadığından, süt veren annelerde kullanılması önerilmez.
Yan Etkileri:
Yan etkiler genellikle nadir görülüp, en sık olanları uyuşukluk ve ağız kuruluğudur. Bulantı, kusma, terleme, hipotansiyon, sersemlik hissi, hipersensitivite ve baş ağrısı nadiren bildirilmiştir. Antikolinerjik etkilerine bağlı olarak yaşlılarda üriner retansiyon, konstipasyon, akomodasyon bozuklukları ve mental konfüzyon görülebilir.
İlaç Etkileşimleri:
Narkotik ve narkotik olmayan analjezikler, barbitüratlar, trankilizan ve hipnotikler gibi MSS depresanları veya alkol ile birlikte kullanıldığında hidroksizinin potansiyelize edici etkisi göz önünde bulundurulmalı ve bireysel doz ayarlaması yapılmalıdır. MAO inhibitörleri veya antikolinerjik etkinliği bilinen ilaçlarla birlikte kullanımından kaçınılmalıdır. Hidroksizin fenitoinin antikonvülsan etkinliğini ve adrenalinin presör etkisini azaltır. Hidroksizinin atropin, belladon alkaloidleri, dijitaller, hipotansif ilaçlar veya H2 reseptör antagonistleri ile etkileşimi yoktur.
ZALVOR Saç Kremi
Permetrin 1 %
Piyasa Şekilleri:
59 ml'lik plastik şişelerde.
Kullanım Şekli:
Erişkin ve 6 ayın üzerindeki çocuklarda normal şampuanla yıkanan ve sonra havlu ile kurulanmış saçlara saç ve kafa derisi tamamen kaplanıncaya kadar sürülür. 10 dakika beklendikten sonra bol suyla yıkanır, havlu ile kurutulur. Aynı işlem 1-2 hafta sonra tekrarlanır.
Endikasyonları:
Uyuz tedavisi ve pubis ve baş biti enfestasyonlarının tedavisinde ve risk altındaki insanların bit enfestasyonlarından korunmasında kullanılır.
Kontrendikasyonları:
Piretroidler, piretrinler ve permetrine karşı allerjisi olanlarda kontrendikedir.
15.06.2009
Triptilin (Generic name – Amitriptyline)

TRIPTILIN 25 MG 40 TABLET
Psikoleptikler ve antidepressanlar
Prospektüs Bilgileri:
25mg Amitriptilin hcl Film tablet 1
10mg Amitriptilin hcl Film tablet 1
Endikasyonları:
Triptilin gerek endojen gerekse eksojen tabiatta psikoz yada nevrozların belirtisi olan depresyonda başarı ile kullanılır.
Kontrendikasyonları:
Glokomda ve idrar tutukluğunda kontrendikedir.
Uyarılar / Önlemler:
Hayvan deneylerinde fetal malformasyona yol açmadığı gösterilmiş isede klinik denemeler sınırlı olsuğundan gebelerde tavsiye edilmez. Diğer ilaçların etkisini potansiyalize eden MAO inhibitörleriyle birlikte kullanılmamalıdır. Ancak bu ilaçlar kesildikten bir hafta sonra tedaviye ihtiyatla başlanmalı doz tedricen arttırılmalıdır. Ağı depresyonlar da, hastalığın icadı olarak intihar ihtimali olduğu hatırdan çıkarılmamalı ve bu gibi hastalar tam bir iyileşme olana kadar yakından izlenmelidir.
Yan Etkiler:
Genellikle hafif olduğundan Triptiline iyi tahamül edilir. Bazı hastalarda uyuklama görülsede aşikar anksietesi olan hastalarda nadirdir. Uyuklama tedaviye ndevam edildiğinde birkaç gün içinde kaybolabilir. Ayrıca baş dönmesi, bulantı, taharrüşiyet, hipotansiyon, ince tremor, haisizlik, asabiyet, baş ağrısı, mide yanması, terleme, etrafta uyşukluk, antikolinerjik agtivitesine bağlı olarak taşikardi, ağız kuruluğu, görme bulanıklığı, idrar tutuklığu, kabızlık bildirilmiştir. Diğer antidepresifler gibi latent bir şizofreninin alevlenmesine yol açabilir.
Etkileşimler:
Canlı vürüs aşılarının immunglobulin uygulamasından ve kan transfüzyonundan sonra inaktive olmaları nedeni ile, böyle uygulamalardan sonra en az 6 hafta süreyle aşı uygulanmamalıdır. Benzer şekilde kızamık, kızamıkçık ve kabakulak aşı uygulamasından sonra iki hafta süreyle immunglobulin uygulanmamalıdır.
Dozu Kullanma:
Başlangıç tedavisi tedaviye günde üç defa 25mg ile başlanır. Gerekirse doz arttırır. Günlük total dozun 150mg geçmesi enderdir. Yaşlı kimselerde ve gençlerde daha küçük dozlarda tedavi sağlanır. Hastanede yatan hastaların küçük bir yüzdesinde memnuniyet verici cevap almak için 300mg kadar çıkmak gerekebilir. Triptili’nin trankilinas etkisi derhal görülür. Antidepresif etkisi ise 3-4 gün içinde başlar elverişli bir cevap 30 gün gecikebilir.
Etken Maddesi: Amitriptilin HCL
TRIPTILIN 25 MG 40 TABLET Yerli, Beşeri bir ilaçdır.
Faverin
FAVERIN 100 MG 30 TABLET
Nöropsikiyatrik » Serotonin re-uptake inhibitörü, Antidepresan
Prospektüs Bilgileri:
Fluvoksamin maleat, 100 mg
Endikasyonları:
Depresyon ve depresif belirtilerin tedavisinde. • Obsesif-kompulsif bozukluk belirtilerinin tedavisinde.
Kontrendikasyonları:
Etken maddeye aşırı duyarlılık durumunda.
Uyarılar / Önlemler:
MAO inhibitörleri ile birlikte kullanılmamalıdır. Hepatik yetmezliği olan hastalarda dikkatle kullanılmalıdır. Kesin gerekli görülmedikçe epileptik hastalarda ve gebelerde kullanılmamalıdır. Hastaların alkol kullanmaktan kaçınmaları önerilmelidir.
Yan Etkiler:
Bulanık görme, ağız kuruluğu, bulantı, kusma, uyuklama, konstipasyon, iştahsızlık ve tremor gibi yan etkiler görülebilir.
Etkileşimler:
Karaciğerde oksidayon yolu ile metabolize olan ilaçların eliminasyon sürelerini uzatabilir. Terapötik indeksi dar olan ilaçlarla warfarin, fenitoin, teofilin, klozapin ve karbamazepin gibi ilaçlarla klinikte önem taşıyan etkileşmeler görülebilir.Trisiklik antidepresanlarla birlikte kullanımı önerilmez.Propranololun plazma düzeylerinde yükselmeye yol açabilir. Lityum, fluvoksaminin seratonerjik etkilerini arttırabileceğinden birlikte kullanılacaksa dikkat gerekir.
Dozu Kullanma:
Depresyon Başlangıç olarak akşamları bir defada alınan 50 mg ya da 100 mg’lık dozlar önerilir. Etkili doza ulaşana kadar dozun giderek artırılması önerilir. Etkili günlük doz, genellikle 100 mg’dır ve hastadan alınan yanıta göre ayarlanmalıdır. Doz günde 300 mg’a kadar yükseltilebilir. 150 mg’dan yüksek dozlar, bölünerek verilmelidir. Dünya Sağlık Örgütü’nün (WHO) önerilerine göre, depresif bir dönemin iyileşmesinden sonra en az 6 ay süreyle antidepresan ilaç tedavisine devam edilmelidir. Obsesif-kompulsif bozukluk Başlangıç olarak 3-4 gün süreyle akşamları bir defada alınan 50 mg’lık bir doz önerilir. Etkili günlük doz, genellikle 100-300 mg’dir. Etkili doza ulaşana kadar ve maksimum 300 mg olacak şekilde dozun giderek artırılması önerilir.150 mg’a kadar olan günlük dozlar tercihen akşamları olmak üzere bir defada verilebilir. 150 mg’dan yüksek dozlarin iki ya da üçe bölünerek verilmesi önerilir. Yanıt iyi ise, tedaviye hastaya göre ayarlanmış dozlarda devam edilebilir. On haftalık tedaviden sonra düzelme görülmezse, fluvoksamin tedavisine devam edip etmeme konusu yeniden değerlendirilmelidir. Obsesif kompulsif bozukluk durumunda fluvoksamin tedavisine ne kadar süreyle devam edileceği konusu sistematik olarak araştırılmamasına rağmen, hastalığın kronik niteliği nedeniyle yanıt alınan hastalarda tedaviye on haftadan daha sonra da devam edilmesi mantıklı bir yaklaşım olacaktır. Hastanın etkili en düşük dozu almasını sağlayacak şekilde bireysel doz ayarlamaları yapılmalıdır. Düzenli aralarla tedaviye devam edip etmeme konusu değerlendirilmelidir. Bazı hekimler ilaç tedavisine yanıtı iyi olan hastalarda, ilaç tedavisi ile birlikte davranış psikoterapisi yapılmasını gerekli bulmaktadır. Karaciğer ve böbrek yetmezliği olan hastalarda düşük dozlarda başlanmalı ve tedavi sırasında hastalar dikkatle izlenmelidir. Tabletler çiğnenmeden bir miktar suyla yutulmalıdır.
Etken Maddesi: Fluvoxamine Maleate
FAVERIN 100 MG 30 TABLET Yerli, Beşeri bir ilaçdır.
Desyrel

DESYREL 100 MG 30 TABLET
Sinir Sistemi, Nöroloji >>> Antidepresan
Prospektüs Bilgileri:
Desyrel® 100 mg tablet; Bir tablet, 100 mg trazodon HCl içerir. Desyrel® 50 mg tablet; Bir tablet, 50 mg trazodon HCl ayrıca gün batışı sarısı lak içerir.
Endikasyonları:
Anksiyete ile birlikte olan veya olmayan muhtelif tipte depresyonlar (Endojen, envolusyonel, organik, nörotik, psikoreaktif, atipik sekonder vs.); psikosomatik bozukluklar. – Yaşlıların emosyonel affektif bozuklukları ve organik beyin sendromları.
Kontrendikasyonları:
Trazodona aşırı hassasiyeti olanlarda ve miyokard infarktüsünün başlangıç iyileşme safhalarında kullanılmamalıdır.
Uyarılar / Önlemler:
İntihar fikirlerinin depresyon iyice düzelinceye kadar devam edeceği göz önünde tutulmalı, hastaya fazla ilaç yazılmamalı ve kontrol altında bulundurulmalıdır. Hastalar, makine ve vasıta kullanma gibi tehlikeli işleri yapmak için gerekli zihni ve fiziki yeteneklerinin ilacın etkisiyle azalabileceğinden haberdar olmalıdır. Hastalar, sebepsiz veya olağandan uzun süreli penis ereksiyonu (Priapizm) olduğu takdirde, ilacı kesip hemen doktora başvurmaları konusunda uyarılmalıdır. 24 saatten uzun süren vakalarda ürolog ile konsültasyon zorunludur (bkz. Yan etkiler; Aşırı doz ve tedavisi). Önceden kalp hastalığı olanlarda Desyrel® aritmiye sebep olabileceğinden bu gibi hastalar yakından izlenmelidir. Ateş, boğaz ağrısı ve diğer enfeksiyon belirtisi görülenlerde akyuvar ve mutlak nötrofil sayısı kontrol edilmeli ve düşükse ilaç kesilmelidir. ÇOCUKLARDA: 18 yaşından küçüklerde etki ve emniyeti konusunda yeterli çalışma yoktur. GEBELERDE: Ancak beklenen fayda fetusa muhtemel tehlikeden önemli bulunursa kullanılmalıdır. EMZİRENLERDE: Hayvanlarda süte geçtiği bilindiğinden dikkatli olunmalıdır.
Yan Etkiler:
Desyrel®’in ağız kuruluğu, görme bulanıklığı, bağırsak hareketlerinde bozulma, idrar akımında gecikme, göz içi basıncı artması gibi antikolinerjik yan etkileri, mevcut trisiklik antidepressan ilaçlarınkine oranla çok daha hafif ve seyrektir; plasebo tedavisi görenlerden anlamlı farklılık göstermez. Kardiyovasküler etkiler dahil olmak üzere diğer yan etkiler de trisiklik antidepressanlardan daha seyrektir. İstenmeyen etkiler, genellikle günde 300 mg’dan yüksek dozlarda ve tedavinin ilk birkaç haftasında görülmekte, zamanla dozun azaltılması veya tarifenin değiştirilmesiyle önlenebilmekte ve oldukça nadiren tedavinin kesilmesini gerektirmektedir. Sinir sistemiyle ilişkili yan etkiler, sık olarak tedavinin ilk haftasında görülür ve özellikle uyku hali şeklinde olur. Diğerleri arasında baş ağrısı, baş dönmesi, sersemlik, yorgunluk, asteni, konsantrasyon güçlüğü, sinirlilik, öfke, uykusuzluk, konfüzyon, oryantasyon bozukluğu, hafıza zaafiyeti sayılabilir. Eksitasyon, ajitasyon, hipomani, tonik-klonik nöbetler, kabus, tremor, parestezi, akatizi nadiren bildirilmiştir. Sindirim sistemiyle ilişkili yan etkiler; ishal, bulantı, kusma, ağızda kötü tat, mide ve karında sıkıntı hissidir. Kardiyovasküler yan etkiler arasında hipotansiyon, hipertansiyon, ortostatik hipotansiyon, taşikardi, çarpıntı, nefes darlığı, senkop ve uzun süreli tedavilerde bradikardi sayılabilir. Seksüel sistemle ilişkili olarak libido azalması ve retrograd ejakülasyon bildirilmiştir. Ayrıca cilt döküntüsü, kaşıntı, kilo alma veya verme, kulak çınlaması, ödem, nazal konjesyon, konuşma güçlüğü, aritmi ve lökopeni nadiren görülebilir. Trazodon HCl (Desyrel®) ile tedavi sırasında yaklaşık 9000′de 1 erkek hastada priapizm bildirilmiş ve advers etki trazodonun alfa adrenolitik etkisine bağlanmıştır (bkz. Uyarılar; Aşırı doz ve tedavisi). İlaç kesilince priapizmin % 48.3 hastada kendiliğinden, % 15.6 hastada tıbbi tedavi ile, % 26.4 hastada cerrahi tedavi ile düzeldiği açıklanmış, % 11.2 hastada sonuç bildirilmemiştir. Ayrıca hastaların yarısından fazlasının Desyrel® ile birlikte alkol, uyuşturucu, psikotrop veya diğer ilaçları kullandıkları saptanmıştır. Priapizmin diğer sebeplerle genel insidansı, 20-40 binde bir olarak bildirilmiştir.
Etkileşimler:
Alkol, diğer psikotrop ve merkezi sinir sistemi depressanları ile hipotansif ajanların etkisini artırabileceği hesaba katılmalıdır. MAO inhibitörleri ile etkileşmesi bilinmediğinden katekolamin uptake’ine ve tyramine cevaba etkisi olmamasına rağmen birlikte kullanılmaması ve MAO inhibitörü tedavisi kısa süre önce kesilenlerde Desyrel® tedavisine az dozla başlanıp yavaş bir şekilde artırılması uygundur. ECT tedavisi ile birlikte kullanılmamalıdır. Serum digoksin ve fenitoin konsantrasyonunu artırıcı etkisi hesaba katılmalıdır. Genel anesteziklerle etkileşimi konusu az bilindiğinden, cerrahi müdahalelerden önce Desyrel® tedavisinin kesilmesi uygundur. Yemekle birlikte alınması zirve plazma konsantrasyonunu düşürdüğünden (bkz. Farmakoloji) buna bağlı baş dönmesi, sersemlik gibi yan etkileri azaltır.
Dozu Kullanma:
Desyrel® günde 2-3 defaya bölünmüş dozlar halinde, tercihen yemeklerden sonra alınmalıdır. Sedatif etki yönünden günlük dozun önemli bölümü veya tamamı yatarken verilebilir. Başlangıç dozu, genellikle 50-150 mg arasındadır. Doz; hastalığın ciddiyetine, hastanın genel durumuna, yaş ve kilosuna göre yavaş bir şekilde artırılır. Endojen depresyonlarda ve ciddi depresyonlarda; günde 300-600 mg, Psikojen ve orta derecede ciddi depresyonlarda; günde 150-300 mg, Hafif anksiyeteli depresyon, psikosomatik bozukluk ve geriatride; günde 100-150 mg’dır. Semptomatik iyileşme ilk haftada; optimal antidepressan etki ise ikinci haftada görülür. Ortalama idame dozu, 200 mg’dır. Hastalığın tabiatına göre tedaviye bir süre (Endojen depresyonlarda aylarca) devam edilir. Tedavi, dozun yavaşça azaltılmasıyla kesilmelidir. DOZ AŞIMI ve TEDAVİSİ Aşırı doz, bildirilen yan ve istenmeyen etkilerin sıklık ve şiddetini artırır. 7.5 ve 9.2 g alan iki hastada yalnız uyku hali ve letarji olmuş ve sekelsiz iyileşmişlerdir. Ancak alkol ve diğer merkezi sinir sistemi depressanları ile aşırı dozda alındığında ölüm bildirilmiştir. Böyle durumlarda hastaların yatırılması, midelerinin boşaltılması, semptomatik ve destekleyici tedavilerin uygulanması gerekir. Priapizm görülenlerde ilk 24 saatte tıbbi tedaviler denenebilir. Örneğin, uzman ve tekniği iyi bilen bir hekim tarafından, adrenerjik uyarının hayati fonksiyonlara muhtemel yan etkilerini devamlı izleme imkanı olan bir merkezde her iki korpus kavernozumdan sırayla yaklaşık 20 ml kan alınarak, yerine aynı miktar alfa adrenerjik ilaç içeren solüsyon (1 mcg/ml noradrenalin) verilmesinin iyileşmeyi sağladığı bildirilmiştir. 24 saatten uzun süren priapizm vakalarında tıbbi tedaviler denenmeden ürolog ile konsültasyon zorunludur.
DESYREL 100 MG 30 TABLET Yerli, Beşeri bir ilaçdır
FULSAC

FULSAC 20 MG 16 KAPSUL
Sinir Sistemi, Nöroloji >>> Antidepresan
İlacın Etken Maddesi : Fluoksetin HCL
Prospektüs Bilgileri:
Bir kapsülde ; Fluoksetin 20 mg. (Fluoksetin HCl halinde) Kapsül boyası olarak titandioksit, indigotin ve tartrazin ihtiva eder.
Endikasyonları:
FULSAC Kapsül major depresyonda endikedir.
Kontrendikasyonları:
Fluoksetine ve bileşiminde bulunan diğer maddelere karşı duyarlı (allerjik) hastalarda kullanılmamalıdır.
Uyarılar / Önlemler:
Nöbet hikayesi olan hastalar ve intihar girişimi olasılığı bulunan ağır depresif hastalar tedavi sırasında dikkatle izlenmelidir. Metabolizma değişikliklerinde yol açabilen veya kardiyak, renal ve hepatik rahatsızlıklar gibi hemodinamik cevapları değiştirebilen hastalarda özenle kullanılmalı, merkezi sinir sistem rahatsızlığı olanlar ile bu rahatsızlığa karşı diğer ilaçların kullanılkdığı durumlarda fluoksetin kullanan hastalar yakından izlenmelidir.Fulsac MAO inhibitörleri ile beraber kullanılamaz, hatta MAO inhibitörü terkedilip aradan 2 hafta geçmedikçe (MAO temizleme dönemi) Fulsac verilmez. Eğer Fluoksetin terkedilip MAO inhibitörlerine geçilecek ise en az 5 hafta beklenmelidir.(Fluoksetin temizleme dönemi). Aksi halde (Fulsasc’tan 1 hafta sonra) çok ciddi yan etkiler kaçınılmazdır.Seyrek bile olsa döküntü ve ürtiker görülen hastalarda ilaç terkedilmelidir. Düşük kilolu deprasif hastalarda zayıflamaya neden olabilir.Fulsac alkolle birlikte kullanılmamalıdır. Motorlu araç ve mekanik cihazları kullananlar dikkatli olmalıdır. Fulssac kan şekeri seviyesini etkileyebilir,antidiabetik ilaç dozu ihtiyaca göre düzenlenmelidir. Bileşiminde bulunan tartrazin nedeniyle aşırı duyarlılık reaksiyonları gelişebilir.Gebelerde:Güvenirliği kesinleşmediğinden hekim önerisi yoksa kullanılmamalıdır.Emzirme dönemlerinde:Kesin olarak gerekmedikçe kullanılmamalıdır.Çocuklarda ve yaşlılarda:Faydası ve güvenirliği henüz araştırılmamıştır. Hekime danışmadan kullanılmamalıdır.
Yan Etkiler:
En sık karşılaşılan yan etkiler: Sinirlilik ,uykusuzluk ,yorgunluk, ya da asteni, terleme, anoreksi, bulantı, diyare ,baş dönmesi ,tad değişikliği ,görme bozukluğu ,az oranda ateş ,bacak ağrısı , nazalkonjesyon ,farenjit ,sık idrara çıkma ,seksüel diskfonsiyon bildirilmiştir.
Etkileşimler:
Fulsac MAO inhibitörleri ile beraber kesinlikle verilemez.(uyarılar kısmına bakınız). Bazı kişilerde diazepamin yarılanma süresini uzatabilir. Birlikte kullanılması durumunda lityum düzeyini değiştirebilir. Diğer antidepresanlarla aynı zamanda kullanımı bu ajanların stabl kan düzeyini iki katına çıkarabilir.Antikoagülanlar ve digital gibi proteinlere afinitesi yüksek olan ilaçlarla kullanımı dikkat gerektirir.
Dozu Kullanma:
Hekim başka bir öneride bulunmaz ise Fulsac Kapsül’ün günde 1 defa ve sabah alınması yeterlidir.Gıda ,emilimini geciktirebilir fakat emilen miktar aynı kalır. Aç veya tok iken alınabilir. Beklenen antideprasif etki diğer türevlerde olduğu gibi 4 ila 5 haftalık uzun bir tedavi döneminden sonra sağlanır. Bu durum hasta ve çevrasine hatırlatılmamalıdır. Akut durum düzeltildikten sonra genellikle tedavi ileriye doğru sürdürülmemelidir. Doz bazı kişilerde günde 80 mg.’a kadar arttırılabilirsede günde 20 mg.’lık tek dozun yeterli olduğu uygulamalardan anlaşılmıştır. Günde 20 mg.’ı aşan dozlar bölünerek verilmelidir. Karaciğer ve böbrek problemi olan hastalarda ve diğer ilaçları kullanan yaşlı kimselerde dozun azaltılması önerilmektedir.
REMERON ( Mirtazapin )
REMERON ORAL 15 MG 66 ML SOLÜSYON
Nöropsikiyatrik —>>> Antidepresan
Etken Maddesi Mirtazapin
İthal, Beşeri bir ilaçdır.
Mitazapine, 15 mg/ml (Solüsyon ) , 30 mg (film tablet)
Prospektüs Bilgileri:
Endikasyonları:
Major depresyon epizodları.
Kontrendikasyonları:
Mirtazapine aşırı duyarlık.
Uyarılar / Önlemler:
Hekime danışmadan kullanılmamalıdır. Antidepresanların çoğu ile yapılan tedavi esnasında genelde granülositopeni ya da agranülositoz şeklinde kendini gösteren kemik iliği depresyonu bildirilmiştir. Bu reaksiyonlar çoğunlukla tedavinin 4-6′ıncı haftasında ortaya çıkar ve tedavinin kesilmesi ile geriye döner. İlaç ile yapılan klinik çalışmalar sırasında nadir de olsa reversbl agranülositoz bildirilmiştir. Hekimler, ateş, boğaz ağrısı, stomatit veya diğer enfeksiyon belirtilerine benzer semptomlara karşı dikkatli olmalı, benzer septomlar görüldüğünde tedavi kesilmeli ve kan testleri yapılmalıdır.
Aşağıdaki hastalıklarda doz dikkatle uygulanmalı ve hasta düzenli olarak izlenmelidir;
- epilepsi ve organik beyin sendromu; klinik deneyler sonucunda ilaç ile tedavi gören hastalarda ataklar nadiren görülmektedir.
- hepatik veya renal yetmezlik
-ilati bozukluğu, anjina pektoris ve yakın zamanda geçirilmiş miyokard enfarktüsü gibi kalp hastalıkları; normal önlemler alınmalı ve birlikte kullanılan ilaçlar dikkatle uygulanmalıdır.
-düşük kan basıncı,
Diğer antidepresanlarda olduğu gibi aşağıdaki hastalıklarda dikkatli olunması gerekir:
-prostat hipertrofisine olduğu gibi miktürasyon bozuklukları ,
- akut dar açılı glokom ve intra-oküler basınç artışı,
- diabets mellitus.
Eğer sarılık meydana gelirse tedaviye son verilmelidir. Ayrıca tüm anti-depresanlarda olduğu gibi aşağıdaki hususlar dikkate alınmalıdır:
-şizofren veya diğer psişik bozukluğu olan hastalarda anti-depresan uygulaması ile psişik semptomlarda kötüleşme görülebilir, paranoid düşünceler şiddetlenebilir.
-manik-depresif psikozun depresif fazının tedavisi sırasında manik faza geçiş olabilir.
-intihar girişimi ihtimali göz önünde bulundurularak özellikle tedavinin başlangıcında hastaya sınırlı sayıda ilaç tableti verilmelidir.
-antidepresanlar bağımlılık yapmakla birlikte uzun süreli kullanımdan sonra tedavinin aniden kesilmesi sonucunda bulantı, baş ağrısı ve halsizlik görülebilir.
-Yaşlı hastalar, özellikle yan etkileri açısından antidepresanlara karşı daha hassasdırlar. İlaç kinik çalışmaları sırasında yaşlı hastalarda bildirilen yan etkiler diğer yaş gruplarına oranla daha sık olmamakla birlikte bu ana kadarki tecrübede sınırlıdır.
Gebelikte emzirme döneminde kullanımı: Gebelerde sadece kesin endikasyonunda ve risk/yarar dengesi göz önünde bulundurularak verilebilir. Mirtazapinin anne sütüne geçip geçmediği ile ilgili bilgiler, çocuğun karşılaşacağı riski ölçmek için yetersizdir.
Araba ve makina kullanma üzerine etkisi: İlaç konsantrasyon ve uyanıklık durumunu bozabilir. Antidepresan tedavisi gören hastalar araba sürme ve makine kullanma gibi tahlike potansiyeli olan ve uyanıklık ve konsantrasyon gerektiren işleri yapmaktan kaçınmalıdırlar.
Yan Etkiler:
Depresyonlu hastalarda doğrudan hastalıkla ilgili birtakım semptomlar görülür. Bu yüzden bazen hangi semptomların hastalığa hangilerinin ilaç tedavisine bağlı olduğundan emin olmak güç olabilir. İlaç tedavisi sırasında en çok bildirilen yan etkiler şunlardır:- iştah ve kilo artışı,-uyuklama/sedasyon, genelde tedavinin ilk haftaları içinde görülür. Nadiren aşağıdaki yan etkiler görülebilir:ortostatik hipotansiyon, mani, -konvulsiyon atakları, tremor, miyoklonüs,- ödem ve ödeme bağlı kilo artışı,- akut kemik iliği depresyonu, -enzim düzeylerinde artış, – serum transaminaz aktivitelerinde artış, -deri döküntüsü. Beklenmeyen bir etki görüldüğünde doktorunuza başvurunuz.
Etkileşimler:
Mirtazipin alkolün santral sinir sistemini baskılayıcı etkisini artırabilir. İlaç tedavisi sırasında hastalara alkol alımından kaçınmaları önerilmelidir. – İlaç inhibitörleri ile birlikte veya bu ajanlarla tedavinin kesilmesinden sonraki iki hafta içinde kullanılmalıdır.- Mirtazipin benzodiazepinlerin sedatif etkilerini artırabilir. Bu gruba giren ilaçlar Remeron ile birlikte verildiğinde bu hususa dikkat edilmesi gerekir.
Dozu Kullanma:
Tabletler bir miktar sıvı ile yutularak alınmalı, çiğnenmemelidir. Yetişkinler: Tedavini başlangıç dozu günde 15 mg’dır. Optimal kilinik cevabın alınabilmesi için genelde dozun arttırılması gerekir. Efektif günlük doz genelde 15-45 mg arasındadır. Yaşlılar: Önerilen dozlar yetişkinler ile aynıdır. Yaşlılarda doz artımını tatminkar ve emniyetli bir cevap alınıncaya kadar hasta yakından izlenmelidir. Çocuklar: Çocuklarda ilac’ın güvenlik ve etkinliği belirlenmediğinden çocukların ilaç ile tedavisi önerilmez. Renal ve hepatik yetmezliği olan hastalarda: Mirtazapin klirensi azalabilir. Bu tür hastalara ialç verildiği zaman bu husus göz önünde bulundurulmalıdır. Mirtazipin 20-40 saattlik bir yarılanma ömrüne sahiptir ve dolayısıyla günde tek doz uygulaması uygundur. tercihen, yatmadan önce tek doz alınmalıdır. İlaç gün içinde eşit olarak bölünmüş dozlarda bir sabah bir akşam verilebilir. tedavi 4-6 ay boyunca ve semptomlar tamamen ortadan kalkıncaya kadar sürdürülmelidir. daha sonra tedavi doz giderek azaltılarak kesilebilir. Uygun doz verildiği taktirde tedaviye 2-4 hafta içinde olumlu cevap alınabilir. Yetersiz cevap halinde doz maksimuma kadar çıkarılabilir. İkinci bir 2-4 haftalık dönemden sonra cevap alınmıyorsa tedavi kesilmelidir.
İLAÇ EŞDEĞERLERİ
MİRTARON 30 MG 14 FİLM TABLET
REMERON 30 MG 14 TABLET
MİRTARON 30 MG 28 FİLM TABLET
REMERON 30 MG 28 TABLET
Edronax 4 mg Tablet
FORMÜLÜ:
Herbir Edronax 4 mg Tablet, 4 mg Reboksetin’e eşdeğer 5.224 mg
Reboksetin metansülfonat içerir.
FARMAKOLOJİK ÖZELLİKLERİ:
Farmakodinamik özellikleri:
Reboksetin, noradrenalinin son derece selektif ve güçlü bir geri alım
inhibitörüdür.
Noradrenalin geri alımının inhibisyonu sonucunda sinaptik aralıkta
noradrenalin düzeyinin artması ve noradrenerjik iletinin modifikasyonu, bilinen antidepresan ilaçların en önemli etki mekanizmaları arasında yer almaktadır.
In vitro çalışmalar, Reboksetin’in adrenerjik (α1, α2, β) ve muskarinik
reseptörlere anlamlı derecede afinitesinin olmadığını göstermiştir. Diğer
antidepresan ilaçların, bu tür reseptörlere bağlanmaları nedeniyle
kardiyovasküler, antikolinerjik ve sedatif yan etkilerinin ortaya çıktığı
açıklanmıştır.
Reboksetin, terapötik dozlarda, histamin ve dopamin reseptörlerine önemli
derecede bağlanmamaktadır.
Sağlıklı gönüllülerde, Reboksetin’in 1 ve 3 mg’lık tek dozlarının verilmesini
takiben, doza bağlı EEG modifikasyonları (fronto-santral derivasyonlarda teta
ve hızlı beta dalgalarında azalma) ve performansta iyileşme ile karakterize
(peg-board testi) Santral Sinir Sistemi (SSS) belirtileri görülmüştür.
Farmakokinetik özellikleri:
Sağlıklı genç ve yaşlı gönüllülerde, depresyonlu hastalarda, böbrek ya da
karaciğer yetmezliği olan kişilerde tek veya birden fazla dozun oral verilmesinden sonra Reboksetin’in farmakokinetiği incelenmiştir.
Sağlıklı gönüllülere oral olarak 4 mg’lık tek doz Reboksetin’in verilmesinin
ardından 2 saat içerisinde yaklaşık 130 ng/ml’lik pik düzeylere ulaşılmıştır.
Eldeki veriler mutlak biyoyararlanımın en az % 90 olduğunu göstermektedir.
Reboksetin’in plazma düzeyleri yaklaşık 13 saatlik bir yarılanma ömrü ile
monoeksponensiyel olarak azalmaktadır. Beş gün içinde sabit durum koşulları gözlenmiştir. Klinik olarak tavsiye edilen doz aralıklarında farmakokinetiğin doğrusal olduğu kanıtlanmıştır.
Reboksetin’in tüm vücut sıvılarına dağıldığı düşünülmektedir. Reboksetin, ilaçkonsantrasyonuyla önemli derecede ilişkili olmaksızın insan plazma
proteinlerine (albumine kıyasla α1-asit glikoproteinine belirgin derecede daha yüksek afiniteyle) % 97 oranında bağlanmaktadır.
Doğrudan idrarla atılan miktar, dozun %78’idir. Dozun %10’u değişmeden
idrarla atılmaktadır.
Reboksetin oral yoldan alındıktan sonra büyük oranda metabolize olur. İlaç,
başlıca etoksifenoksi halkasının hidroksilasyonu ve morfolin halkasının odealkilasyonu ve oksidasyonu ile metabolize olur. İn vitro çalışmalar,
Reboksetin’in metabolizasyonundan, sitokrom P-450’nin izozimi olan
CYP3A4’ün başlıca sorumlu olduğunu göstermiştir. İn vitro çalışmalar,
Reboksetin’in sitokrom P-450’nin izozimleri olan CYP1A2, CYP2C9,
CYP2C19 ve CYP2E1’in üzerinde hiçbir etkisi olmadığını göstermiştir. Yüksek konsantrasyonlarda Reboksetin CYP2D6’yı inhibe etmektedir ancak bu durumun klinik yönden önemi bilinmemektedir. İn vitro çalışmalar,
Reboksetin’in çok zayıf bir CYP3A4 inhibitörü olduğunu göstermektedir.
İlaç rasemik karışım olarak mevcuttur (deneysel modellerde aktif olan her iki enantiyomer bulunmakta; enantiyomerler arasında ne kiral inversiyon ne de farmakokinetik etkileşim görülmüştür). Daha güçlü olan SS enantiyomerin, eşdeğer enantiyomerine kıyasla plazma düzeyleri yaklaşık iki kat daha düşük ve idrarla atılımı iki kat daha yüksektir. Bu iki enantiyomerin terminal yarılanma ömürleri arasında anlamlı hiçbir fark gözlenmemiştir.
Yaşlılarda ve böbrek yetersizliği ya da orta ile ağır şiddette karaciğer
yetmezliği olan hastalarda sistemik etkilenim ve yarılanma ömründe artış
belirlenmiştir.
ENDİKASYONLARI:
Reboksetin, depresyonun akut tedavisinde ve başlangıç tedavisine yanıt
vermiş hastalarda klinik iyileşmenin devamını sağlamada endikedir.
KONTRENDİKASYONLARI:
Formülde bulunan Reboksetin veya diğer maddelere karşı aşırı duyarlılık.
UYARILAR/ÖNLEMLER:
— Klinik çalışmalarda nadiren de olsa epileptik nöbet vakaları
görüldüğünden, daha önceden konvülsif hastalığı olduğu bilinen kişilere
Reboksetin, sıkı gözetim altında verilmeli ve hastada nöbet geliştiğinde
kullanımı kesilmelidir.
— MAO inhibitörlerinin Reboksetin ile birlikte kullanımından kaçınılmalıdır.
— Tüm antidepresanlarla olduğu gibi mani/hipomaniye geçişler olmuştur.
Bipolar hastaların yakın takip altına alınması önerilir.
— İntihar girişimi riskine depresyonda doğal olarak rastlanabilir ve bu risk
belirgin bir iyileşme meydana gelene kadar sürer; tedavinin başlangıç
döneminde hastanın yakın takibe alınması önerilir.
— İdrar retansiyonu ve glokom hikayesi olan hastalarda dikkatli olunması
tavsiye edilir.
— Önerilen maksimum dozun üzerindeki dozlarda, ortostatik hipotansiyon
daha sık görülmüştür. Reboksetin, kan basıncını düşürücü etkisi olduğu
bilinen ilaçlarla birlikte uygulandığında yakın takip önerilir.
Gebelerde kullanımı:
Gebelerde yeterli ve kontrollü çalışma bulunmadığından yarar/risk oranı
değerlendirilerek kullanılmalıdır.
Emzirme dönemi:
Reboksetin’in insan sütüne geçip geçmediği bilinmediğinden emziren
annelere verilmesi tavsiye edilmemektedir.
Araç ve makine kullanmaya etkisi:
Reboksetin bir sedatif değildir. Klinik çalışmalar sırasında, Reboksetin ile
kognitif ya da psikomotor zayıflama gözlenmemiştir.
YAN ETKİLER/ADVERS ETKİLER:
Sekiz hafta veya daha kısa süreli, plasebo kontrollü çalışmalarda, Reboksetin
ile tedavi edilen hastaların yaklaşık % 70’inde ve plasebo ile tedavi edilen
hastaların yaklaşık % 60’ında advers etkiler bildirilmiştir. Advers etkilere bağlı olarak ilacı bırakma oranı Reboksetin ve plasebo ile tedavi edilen hastalar arasında benzer olup, bu oran % 10’dan daha düşük olmuştur.
Plasebo ile tedavi edilen hastalara oranla Reboksetin ile tedavi edilen
hastalarda istatistiksel olarak daha sık görülen advers etkiler şunlardır: ağız
kuruluğu, kabızlık, uykusuzluk, terlemede artış, taşikardi, vertigo, idrar
tutukluğu / retansiyonu ve impotans. İmpotans, esas olarak, günde 8 mg’dan
daha yüksek dozlar ile tedavi edilen hastalarda görülmüştür.
Hayati belirtilerdeki tek modifikasyon, ayakta kalmaya bağlı olarak görülen
taşikardi olmuştur. Erişkin hastalarda, Reboksetin ile tedavi süresince, EKG
kayıtlarında taşikardiden başka hiçbir kalıcı değişiklik görülmemiştir.
8 haftadan daha uzun süren çalışmalarda, Reboksetin ile tedavi gören
hastaların yaklaşık %30’unda ve plasebo ile tedavi edilen hastaların yaklaşık
%25’inde yeni advers etkilere rastlanmıştır.Sekiz haftadan daha uzun süreli
çalışmaların advers etki profili ile, sekiz hafta veya daha kısa süreli
çalışmaların profilleri arasında bir farklılık söz konusu değildir. İlaç kesildiğinde görülen advers etkiler nadirdir; bu durum Reboksetin grubundaki hastaların %4’ünde, plasebo grubundakilerin %1’inde görülmüştür. Reboksetin ile tedavi edilen grupta daha sık olarak gözlenen tek yan etki kabızlık olmuştur.
Tedavinin kesilmesi sırasında görülen advers etkiler nadir olup, Reboksetin ile tedavi edilen hastaların yaklaşık %4’ünde ve plasebo ile tedavi edilenlerin
%6’sında görülmüştür.
İLAÇ ETKİLEŞMELERİ VE DİĞER ETKİLEŞMELER:
— İn vitro çalışmalar, Reboksetin’in CYP1A2, CYP2C9, CYP2C19 ve
CYP2E1 gibi sitokrom P-450 izozimlerinin aktivitelerini inhibe etmediğini
göstermiştir. Yüksek konsantrasyonlarda Reboksetin CYP2D6’yı inhibe
eder, ancak bu gözlemin klinik önemi bilinmemektedir. İn vitro çalışmalar,
Reboksetin’in CYP3A4’ü çok az inhibe ettiğini göstermiştir.
— İn vitro metabolizma çalışmaları, Reboksetin’in esas olarak sitokrom
P450’nin izozimi olan CYP3A4 tarafından metabolize olduğunu
göstermektedir; Reboksetin CYP2D6 tarafından metabolize olmamaktadır.
Bu nedenle, CYP3A4 ‘ün aktivitesini azaltan ilaçların, Reboksetin’in
plazma konsantrasyonlarını artıracağı beklenmektedir. Sağlıklı
gönüllülerde yapılan bir çalışmada, güçlü CYP3A4 inhibitörü olan
Ketokonazol’ün, Reboksetin enantiomerlerinin plazma konsantrasyonlarını
yaklaşık % 50 oranında artırdığı görülmüştür.
— Reboksetin ile Lorazepam arasında anlamlı hiç bir farmakokinetik etkileşim saptanmamıştır.
— Sağlıklı gönüllülerde yapılan bir in vivo çoklu doz çalışmasında,Fluoksetin
ve Reboksetin arasında klinik önem taşıyan bir etkileşim gözlenmemiştir.
— Reboksetin’in sağlıklı kişilerde alkolün kognitif fonksiyonlar üzerindeki
etkisini potansiyelize etmediği düşünülmektedir.
— Reboksetin’in diğer antidepresanlarla (trisiklikler, MAO inhibitörleri,
SSRI’ler ve lityum) birlikte kullanımı klinik çalışmalarla
değerlendirilmemiştir.
— Birlikte alınan gıdalar Reboksetin’in absorbsiyon derecesini anlamlı
derecede etkilemez.
KULLANIM ŞEKLİ VE DOZU:
Edronax 4 mg Tablet oral yoldan kullanılır.
Klinik etkinlik, tedaviye başladıktan 14 gün sonra görülür.
Yetişkinlerde kullanımı
Önerilen terapötik doz, günde iki kez 4 mg (8 mg/gün)’dır.
3 hafta sonra, yeterli klinik yanıt alınamaması durumunda bu doz günde 10
mg’a kadar artırılabilir.
Yaşlılarda kullanımı (65 yaşın üzerinde)
Önerilen terapötik doz, günde 2 defa 2 mg (4 mg/gün)’dır. Reboksetin’e
başladıktan 3 hafta sonra yeterli klinik yanıt alınamaması durumunda, bu doz günde 6 mg’a kadar artırılabilir.
Çocuklarda kullanımı
Çocuklarda Reboksetin kullanımına dair herhangi bir veri mevcut değildir.
Böbrek veya karaciğer yetmezliği olan hastalarda kullanımı
Böbrek ya da orta ile ağır şiddette karaciğer yetmezliği olan hastalarda
başlangıç dozu günde iki defa 2 mg olmalıdır; bu doz hasta toleransına bağlı
olarak artırılabilir.
DOZ AŞIMI VE TEDAVİSİ:
Bazı vakalar için, klinik çalışmalar boyunca, birkaç gün ile birkaç haftaya
varan zaman dilimi içinde, hastalara, tavsiye edilen dozlardan daha yüksek
dozlar (12-20 mg/gün) verilmiştir. Tedavideki acil advers etkiler; postural
hipotansiyon, anksiyete ve hipertansiyon olmuştur.
Kendiliğinden 52 mg’a kadar varan dozlarda Reboksetin kullanmış olan 2
hastada ciddi advers etkiler saptanmamıştır.
Doz aşımı durumunda, kardiyak fonksiyon ve tüm hayati bulgular izlenmelidir.
SAKLAMA KOŞULLARI:
250C’nin altındaki oda sıcaklığında saklayınız.
TİCARİ TAKDİM ŞEKLİ VE AMBALAJ MUHTEVASI:
4 mg Reboksetin’e eşdeğer 5.224 mg Reboksetin metansülfonat içeren 60
tabletlik blister ambalajlarda.
RUHSAT SAHİBİ VE İTHAL EDEN:
Pfizer İlaçları Ltd. Şti. 34347 Ortaköy / İSTANBUL
ÜRETİM YERİ:
Pharmacia S.p.A., İtalya
RUHSAT TARİHİ: 18.02.2005 RUHSAT NO: 117/31
(Prospektüs Onay Tarihi: 23.02.2005)
Çocukların ulaşamayacağı yerlerde ve ambalajında saklayınız.
Reçete ile satılır.
BEKLENMEYEN BİR ETKİ GÖRÜLDÜĞÜNDE DOKTORUNUZA
BAŞVURUNUZ.
Kaynak: http://www.pfizer.com.tr
MİRTARON® 30 mg FİLM TABLET
FORMÜLÜ
Her çentikli film tablette 30 mg mirtazapin bulunur.
Boyar maddeler: Titanyum dioksit (E171), demir oksit sarı (E172) ve FD&C Yellow No: 6 (E 110)
FARMAKOLOJİK ÖZELLİKLER
Mirtazapin, major depresyon tedavisinde kullanılan bir antidepresandır. Anhedoni, psikomotor inhibisyon, uyku düzeninde bozulma (erken uyanma) ve kilo kaybı gibi semptomların varlığı pozitif yanıt alma şansını artırabilir. İlgi kaybı, intihar düşüncesi, (akşamları sabaha oranla daha iyi) duygudurum değişikliği diğer semptomlardır. Mirtazapin etkisini, genellikle, tedavinin başlamasından sonra 1-2 hafta içinde göstermeye başlar.
Farmakodinamik etkiler
Mirtazapin merkezi etkili bir presinaptik α2-antagonistidir, merkezi noradrenerjik ve serotonerjik nörotransmisyonu artırır. Mirtazapin 5-HT2 ve 5-HT3 reseptörlerini bloke ederek 5-HT1 reseptörü üzerinden gerçekleşen serotonerjik nörotransmisyonu güçlendirir.
Mirtazapinin S(+) enantiyomerinin, α2 ve 5-HT2 reseptörlerini; R(-) enantiyomerinin ise 5-HT3 reseptörünü bloke ederek antidepresan etkiye katkıda bulunduğu kabul edilmektedir. Mirtazapinin sedatif özelliklerinden histamin H1 antagonistik aktivitesi sorumludur. Mirtazapin genelde iyi tolere edilen bir ilaçtır. Pratik olarak antikolinerjik etkinliği yoktur ve terapötik dozlarda kardiyovasküler sistem üzerinde herhangi bir etki görülmez.
Farmakokinetik özellikler
Emilim
Tabletlerin oral yoldan kullanılmasından sonra etkin madde mirtazapin hızla ve iyi emilir (biyoyararlanım = % 50 ) ve iki saatte doruk plazma düzeyleri elde edilir. Önerilen dozlarda mirtazapin, doğrusal bir farmakokinetik gösterir. Sabit plazma düzeylerine 3-4 gün sonra ulaşılır ve sonrasında birikim gözlenmez. Gıdalar mirtazapinin farmakokinetik özelliklerini değiştirmez.
Dağılım
Mirtazapin yaklaşık % 85 oranında plazma proteinlerine bağlanır.
Metabolizma Başlıca biyotransformasyon yolakları demetilasyon ve oksidasyondur; konjugasyonla da metabolize olmaktadır. 8-hidroksi metabolitinin oluşumunda sitokrom P450 (CYP) 2D6 ve 1A2; N-demetil ve n-oksit metabolitlerinin oluşumunda ise CYP3A4’ün rolü bulunmaktadır.
Demetil metaboliti farmakolojik olarak etkindir ve ana madde ile benzer bir farmakokinetik profile sahip olduğu düşünülmektedir.
Atılım
Ortalama eliminasyon yarılanma ömrü 20-40 saattir. Yarılanma ömrünün, bazen, 65 saate kadar uzayabildiği ve genç erkeklerde daha kısalabildiği gözlenmiştir. Eliminasyon yarılanma ömrü günde tek doz uygulanmasını mümkün kılar. Mirtazapinin büyük bir kısmı metabolize olarak birkaç gün içinde idrar (%75) ve feçes (%15) ile atılır.
Özel hasta gruplarında özellikleri
Böbrek veya karaciğer yetmezliği mirtazapin klerensini azaltabilir.
ENDİKASYONLARI
Major depresyon epizodlarında endikedir.
KONTRENDİKASYONLARI
Mirtazapine veya bileşimindeki maddelerden herhangi birine karşı aşırı duyarlılığı olanlarda kullanımı kontrendikedir.
UYARILAR/ÖNLEMLER
Hekime danışmadan kullanılmamalıdır.
Antidepresan ilaçların özellikle çocuk ve gençlerdeki kullanımlarının, intihar, düşünce ya da davranışlarını artırma olasılığı bulunmaktadır. Bu nedenle özellikle tedavinin başlangıcı ve ilk aylarında, ilaç dozunun artırılma, azaltılma ya da kesilme dönemlerinde hastanın gösterebileceği huzursuzluk, aşırı hareketlilik gibi beklenmedik davranış değişiklikleri ya da intihar olasılığı gibi nedenlerle hastanın gerek ailesi gerekse tedavi edicilerle yakınen izlenmesi gereklidir.
Çocuklarda olduğu gibi yetişkinlerde de antidepresan ilaçların kullanımı gerektiğinde özellikle ilk 5 ay ve doz değiştirme durumlarında daha fazla olmak üzere, hastaların intihar, düşünce ve davranışlarında artış olasılığı yönünden uyarılması ve yakın takibi gereklidir.
Nadiren, mirtazapinle tedavi esnasında lökopeni, granülositopeni ya da agranülositoz’u da içeren geri dönüşümlü lökosit bozuklukları bildirilmiştir. Bu bozuklular, çoğunlukla, tedavinin 4-6′ıncı haftasından sonra ortaya çıkar ve genellikle tedavinin sonlandırılması ile düzelir. Hekimler, ateş, boğaz ağrısı, stomatit veya diğer enfeksiyon belirtileri gibi agranülositoz semptomlarına karşı dikkatli olmalı, bu tür semptomlar görüldüğünde tedavi
sonlandırılmalı ve kan sayımı yapılmalıdır. Hastalar bu tür semptomlar konusunda bilgilendirilmelidir.
Aşağıdaki hastalarda doz dikkatle uygulanmalı ve hasta düzenli olarak yakından izlenmelidir.
Epilepsi ve organik beyin sendromu: Diğer antidepresanlarda olduğu gibi, epileptik nöbet öyküsü olan hastalarda mirtazapin dikkatle kullanılmalıdır. Nöbet görülen ya da nöbet görülme sıklığı artan hastalarda tedavi sonlandırılmalıdır. Stabil olmayan nöbet/epilepsi hastalarında antidepresanlarla tedaviden kaçınılmalıdır. Kontrol altındaki epilepsi
hastalarında ise antidepresanlarla tedavi sırasında hastaların yakın takibi önerilmektedir. Klinik deneyler sonucunda, mirtazapin ile tedavi gören hastalarda atakların nadiren görüldüğü saptanmıştır.
Karaciğer ya da Böbrek yetmezliği
İleti bozukluğu, anjina pektoris ve yakın zamanda geçirilmiş miyokard enfarktüsü gibi kalp hastalıkları: Normal önlemler alınmalı ve birlikte kullanılan ilaçlar dikkatle uygulanmalıdır.
Kan basıncı düşüklüğü
Diabetes mellitus: Antidepresanlarla tedavi, diyabetik hastalarda, kan şekeri düzeylerini değiştirebilir. İnsülin ve/veya oral hipoglisemik ilaçların dozunun ayarlanması ve hastaların yakından izlenmesi önerilmektedir.
Diğer antidepresanlarda olduğu gibi, aşağıdaki hastalıklarda dikkatli olunması gerekir:
Prostat hipertrofisi gibi işeme bozuklukları (mirtazapinin antikolinerjik etkisi çok zayıf olduğundan herhangi bir problem çıkması beklenmez).
Akut dar-açılı glokom ve göz içi basınç artışı (zayıf antikolinerjik etkiden dolayı problem çıkma olasılığı çok düşüktür).
Eğer sarılık meydana gelirse tedaviye son verilmelidir.
Ayrıca tüm antidepresanlarda olduğu gibi aşağıdaki hususlar dikkate alınmalıdır.
Şizofreni veya başka bir psikotik bozukluğu olan hastalarda psikotik semptomlarda kötüleşme görülebilir; paranoid düşünceler şiddetlenebilir.
Manik-depresif psikozun depresif fazının tedavisi sırasında manik faza geçiş olabilir.
Tüm antidepresanlarda olduğu gibi, özellikle tedavinin ilk bir kaç haftasında iyileşme gözlenmeyebileceğinden, hastalar bu dönemde yakından izlenmelidir. Depresyona bağlı intihar girişimi olasılığı, bariz remisyon gözlenene kadar söz konusu olabilir. Genellikle tüm depresyon tedavilerinde, iyileşmenin ilk safhalarında, intihar girişimi olasılığında artış
olduğu göz ardı edilmemelidir.
Antidepresanlar bağımlılık yapmamakla birlikte, uzun süreli kullanımdan sonra tedavinin aniden kesilmesi bulantı, baş ağrısı ve halsizliğe neden olabilir.
Yaşlı hastalar özellikle yan etkileri açısından antidepresanlara karşı daha duyarlıdırlar. Klinik çalışmalar sırasında yaşlı hastalarda bildirilen yan etkiler diğer yaş gruplarına oranla daha sık olmamakla birlikte, henüz bu konuda deneyim sınırlıdır.
Gebelik ve emzirme döneminde kullanımı
Gebelik kategorisi: C
Gebe kadınların tedavisiyle ilgili yeterli veri olmadığından mirtazapin gebelik sırasında kullanımı önerilmez. Mirtazapin kullanan ve gebe kalma potansiyeli olan kadınlara uygun bir kontrasepsiyon önerilmelidir.
Mirtazapinin insanlarda anne sütüne geçip geçmediği ile ilgili bilgiler yetersiz olduğundan emziren annelerde kullanımı önerilmemektedir.
Araç ve makine kullanma üzerine etkisi
Mirtazapin, özellikle yaşlılarda, geçici sedatif etkilere neden olabilir, başlangıçta konsantrasyonu ve uyanıklık durumunu bozabilir. Mirtazapin kullanan hastalar, araba sürme ve makine kullanma gibi tehlike potansiyeli olan, uyanıklık ve konsantrasyon gerektiren işler
konusunda bilgilendirilmelidirler.
YAN ETKİLER/ADVERS ETKİLER
Depresyonlu hastalarda, doğrudan hastalıkla ilgili bir takım semptomlar görülür. Bu yüzden hangi semptomların hastalığa, hangilerinin mirtazapin tedavisine bağlı olduğundan emin olmak güç olabilir. Mirtazapin tedavisi sırasında sık (> %1) gözlendiği bildirilen yan etkiler şunlardır:
İştah ve kilo artışı
Uyuklama/sedasyon/halsizlik, genelde tedavinin ilk haftaları içinde görülür. (Not: Dozun azaltılması sedasyonun azalmasına yol açmaz fakat antidepresan etkinliği azaltabilir).
Genel ya da lokal ödem Nadiren (> ‰ 1) aşağıdaki yan etkiler görülebilir:
Baş ağrısı, sersemleme
Karaciğer enzim düzeylerinde artış Çok nadiren, geri dönüşümlü agranülositoz, kabuslar, mani, konvülsiyon, tremor, miyoklonus,
parestezi, ortostatik hipotansiyon, döküntü, huzursuz bacaklar, artralji/miyalji gözlenebildiği bildirilmiştir. Ajitasyon ve halusinasyonlar gibi nadiren gözlenen semptomlar altta yatan hastalığa bağlı olarak da ortaya çıkabilir.
Mirtazapin bağımlılığa yol açmadığı halde, uzun süre kullanımdan sonra tedavinin aniden kesilmesi bazı semptomlara neden olabilmektedir. Bu semptomların büyük bir çoğunluğu hafif ve sınırlıdır. Bulantı, anksiyete ve ajitasyon sıklıkla bildirilen semptomlardır. Bu semptomların altta yatan hastalığa bağlı olabileceği de göz önünde bulundurulmalıdır.
Mirtazapin tedavisinin doz azaltılarak sonlandırılması önerilmektedir.
BEKLENMEYEN BİR ETKİ GÖRÜLDÜĞÜNDE DOKTORUNUZA BAŞVURUNUZ.
İLAÇ ETKİLEŞİMLERİ VE DİĞER ETKİLEŞİMLER
Mirtazapin, alkolün merkezi sinir sistemini baskılayıcı etkisini artırabilir. Mirtazapin tedavisi sırasında hastalara alkol kullanımından kaçınmaları önerilmelidir.
Mirtazapin, mono-amin oksidaz inhibitörleri (MAOİ) ile birlikte veya bu ilaçlarla tedavinin sonlandırılmasından sonraki iki hafta içinde kullanılmamalıdır.
Mirtazapin, benzodiyazepinlerin sedatif etkilerini artırabildiğinden, birlikte kullanılmaları gerektiğinde dikkatli olunması gerekir.
In vitro çalışmalar, mirtazapinin CYP 450 1A2, 2D6 ve 3A enzimlerinin zayıf kompetitif inhibitörü olduğunu düşündürmektedir. Bu nedenle, mirtazapinin HIV proteaz inhibitörleri, azol antifungaller, eritromisin ve nefazodon gibi CYP3A4’ün güçlü inhibitörleriyle birlikte kullanımında dikkatli olunmalıdır.
CYP 3A4’ün potent inhibitörü olan ketokonazol ile mirtazapinin birlikte kullanımı, mirtazapinin doruk plazma seviyesini % 30, eğrinin altında kalan alanı da % 45 artırmaktadır.
CYP 3A4’ü indükleyen karbamazepin, birlikte kullanıldığında mirtazapinin klerensini 2 kat artırarak plazma seviyesini % 45-60 oranda azaltmaktadır. Fenitoin de mirtazapinin klerensini benzer şekilde artırmaktadır. Karbamazepin ya da diğer ilaç metabolizmasını hızlandıran
ürünler ile mirtazapin birlikte kullanıldığında, mirtazapinin dozunun artırılması gerekebilir.
Birlikte kullanılan bu ürünler kesildiğinde ise mirtazapinin dozunun azaltılması gerekebilir.
Simetidinle birlikte kullanıldığında mirtazapinin biyoyararlanımı % 50 oranda artmaktadır.
Bu nedenle birlikte kullanıldıklarında mirtazapinin dozunun ayarlanması gerekebilir.
In vivo çalışmalarda mirtazapin, CYP 2D6 ile metabolize olan risperidon ya da paroksetin, CYP 3A4 ile metabolize olan karbamazepin, amitriptilin ve simetidinin farmakokinetik özelliklerini etkilememiştir.
Mirtazapin ve lityumun birlikte kullanımında, klinik etki ya da farmakokinetik özelliklerde herhangi bir değişiklik saptanmamıştır.
Mirtazapin ve seçici serotonin geri-alım inhibitörleri birlikte kullanıldığında, klinik açıdan anlamlı herhangi bir ilaç etkileşimi saptanmamıştır.
St John’s wort, mirtazapin düzeylerini düşürebildiğinden birlikte kullanımlarından kaçınılmalıdır.
Valerian, St John’s wort, SAMe ve kava kava merkezi sinir sistemi depresyonunu artırabilir.
KULLANIM ŞEKLİ VE DOZU
Tabletler bir miktar sıvı ile yutularak alınmalı ve çiğnenmemelidir.
Mirtazapin yarılanma ömrü 20-40 saat olduğundan günde tek doz uygulamasına uygundur.
Tercihen, yatmadan önce tek doz olarak kullanılmalıdır.
Mirtazapin gün içinde sabah ve akşam 2 eşit dozda verilebilir.
Erişkinler:
Tedavinin başlangıç dozu günde 15 mg’dır.
Optimal klinik yanıtın alınabilmesi için genelde dozun artırılması gerekebilir. Efektif günlük doz genellikle 15 ile 45 mg arasındadır.
Yaşlılar:
Önerilen dozlar erişkinlerle aynıdır. Yaşlılarda doz artımında tatminkar ve emniyetli bir yanıt alınıncaya kadar hasta yakından izlenmelidir.
Çocuklar:
Çocuklarda güvenlik ve etkinliği belirlenmediğinden çocukların mirtazapin ile tedavisi önerilmez.
Renal ve hepatik yetmezliği olan hastalarda mirtazapin klerensi azalabilir. Bu tür hastalara mirtazapin verildiği zaman bu konu göz önünde bulundurulmalıdır.
Tedavi, 4-6 ay boyunca ve semptomlar tamamen ortadan kalkıncaya kadar sürdürülmelidir.
Daha sonra tedavi, doz azaltılarak kesilebilir. Uygun doz verildiği takdirde tedaviye 2-4 hafta içinde olumlu yanıt alınabilir. Yetersiz yanıt halinde ilacın dozu maksimum doza kadar çıkarılabilir. İkinci bir 2-4 haftalık dönemden sonra yanıt alınamıyorsa tedavi sonlandırılmalıdır.
DOZ AŞIMI VE TEDAVİSİ
Mirtazapinle doz aşımına ilişkin deneyimler, semptomların genellikle orta düzeyde olduğunu göstermektedir.
Aşırı dozda mirtazapin alımı durumunda, taşikardi ve hafif hiper/hipotansiyonla ile birlikte oryantasyon bozukluğu ve uzun süreli sedasyon gibi merkezi sinir sisteminin baskılanması bulguları söz konusu olabilir.
Aşırı doz alımı halinde gastrik lavaj ve yaşamsal işlevlerin devamı için gerekli semptomatik ve destekleyici tedavi uygulanmalıdır.
SAKLAMA KOŞULLARI
25°C altındaki oda sıcaklığında saklanmalıdır.
Çocukların göremeyeceği ve erişemeyeceği yerlerde ve ambalajında saklayınız.
TİCARİ TAKDİM ŞEKLİ VE AMBALAJ MUHTEVASI
Mirtaron® 30 mg film tablet: 14 ve 28 film tabletlik ambalajlarda.
RUHSAT SAHİBİ
Eczacıbaşı Sağlık Ürünleri San.ve Tic. A.Ş.
Büyükdere Cad. Ali Kaya Sok. No:7
Levent 34394 İstanbul
ÜRETİM YERİ
Eczacıbaşı Sağlık Ürünleri San.ve Tic. A.Ş.
Küçükkarıştıran 39780 Lüleburgaz
Ruhsat tarihi: 11.12.2007
Ruhsat no: 213/70
Prospektüs onay tarihi: 13.12.2007
Reçete ile satılır.
® Tescil edilmiş marka
Kaynak: http://www.eczacibasi-zentiva.com.tr
DEPRENİL 50 mg
Depresyon, depresyona bağlı yeme ve uyku bozuklukları, bipolar hastalığın depresyon fazı, migren
FORMÜLÜ
Her bir Deprenil tablet 50 mg opipramol dihidroklorür içerir.
FARMAKOLOJİK ÖZELLİKLERİ
Farmakodinamik Özellikleri
Opipramol, trisiklik antidepresan bir ilaçtır. Merkezi sinir sisteminde noradrenalin ve serotonin`in sinaptik konsantrasyonlarını yükseltir. Trankilizan ve sedatif özelliklere sahiptir. Sakinleştirici ve mizacı canlandırıcı etkidedir. Antihistaminik aktivitesi belirgin, antikolinerjik etkisi zayıftır. Uzun süreli kullanıldığında, kortikal beta-adrenerjik reseptörler üzerinde down-regulation yapabilir. Bağımlılığa yol açmadan psikosomatik fonksiyonları düzenler.
Farmakokinetik Özellikleri
Opipramol, ağız yoluyla alındıktan sonra tamamen absorbe olur. Tekrarlayan dozlarla 14-64 µg/ml plazma konsantrasyonuna ulaşır. Alınan dozun yaklaşık % 91`i plazma proteinlerine bağlanır. Plazma yarı ömrü 6-23 saat arasıdır. % 70 kadarı idrarla, bir bölümü de feçesle vücuttan atılır. Alınan dozun yaklaşık % 5-9`u değişmeden atılır. Böbrek fonksiyon bozukluğu olan hastalarda atılımı daha yavaştır.
ENDİKASYONLARI
Deprenil ,
Anksiyete, huzursuzluk, uykusuzluk, menopoz döneminden kaynaklanan sıkıntılar, endojen depresyon, depresyona bağlı huy değişiklikleri, depresyonla birlikte seyreden yeme bozuklukları (iştahsızlık veya aşırı iştah), psikosomatik rahatsızlıklarda endikedir.
KONTRENDİKASYONLARI
Opipramol ve diğer trisiklik antidepresanlara karşı aşırı duyarlı olduğu bilinen hastalarda, kalp hastalığı olanlarda, glokomda,idrar retansiyonunda, karaciğer yetmezliği, epilepsi ve alkolizm durumlarında kontrendikedir.
UYARILAR / ÖNLEMLER
· Opipramol dihidroklorür, kardiyovasküler hastalığı olanlarda, epilepsi, prostat hipertrofisi ve karaciğer yetmezliği olan hastalarda dikkatle kullanılmalıdır.
· Deprenil tablet tedavisi süresince alkol alınmamalıdır.
· Deprenil tablet, tedavisi ile Monoaminoksidaz (MAO) inhibitörlerinin kullanılması arasında en az 14 günlük bir ara verilmelidir.
· Alerjik deri döküntülerine rastlandığı takdirde tedavi durdurulmalıdır.
· Tedavi süresince düzenli olarak kan sayımı yapılmalıdır.
· Dar açılı glokomu olan hastalarda, glokomun şiddetlenmesi riski nedeniyle kullanılmaması önerilir.
· Prostat ya da üretraya bağlı sorunlar nedeniyle miksiyon güçlüğü çeken hastalarda idrar retansiyonu riski nedeniyle kullanılmaması önerilir.
· Yakın tarihte miyokard enfarktüsü geçirenlerde, sultoprid tedavisi uygulanan hastalarda kullanılmamalıdır.
· Antidepresan ilaç tedavisine başlanan depresyonlu hastalarda, intihar girişimi riski yüksektir. Bu nedenle tedavi başlangıcında dikkatli olunmalı ve hasta yakından izlenmelidir.
· Şiddetli ve inatçı baş ağrısı, halsizlik, bulantı, anksiyete, uyuma sorunları ile karakterize bir sendrom tablosu görülen ender vakalarda doz azaltılmalı ve bu dönemde hasta yakından izlenmelidir.
· Tedaviye başlangıç döneminde uykusuzluk ya da sinirlilik görülen hastalarda doz azaltılabilir ya da geçici semptomatik tedavi uygulanabilir.
· Ağır manik belirtiler görülen hastalarda opipramol tedavisi kesilmeli ve gerekirse sedatif nöroleptik tedavisine başlanmalıdır.
· Epilepsili hastalarda ya da epilepsi anemnezi bulunanlarda konvülsiyon görülürse opipramol tedavisi kesilmelidir.
· Yaşlı hastalarda ortostatik hipotansiyon ve sedatif etkiler, kronik konstipasyon ve prostat hipertrofisine bağlı miksiyon güçlüğü nedeniyle dikkatli olunmalıdır.
· Kinidin türevi ilaçlar, taşikardik ve hipotansif etkili ilaç kullanan hastalarda, opipramol bu ilaçların etkisini güçlendirebileceğinden dikkatli olunmalıdır.
Gebelikte Kullanımı: Gebelik Kategori B
Gebelikte kullanımıyla ilgili yeterli ve kontrollü çalışmalar yoktur. Sadece doktor gerekli gördüğü takdirde, beklenen terapötik fayda fetüs üzerindeki riskten fazla ise kullanılabilir.
Emziren Annelerde Kullanımı
Terapötik dozu takiben etken maddenin az miktarda da olsa süte geçtiği saptanmıştır.
Araç ve Makine Kullanmaya Etkisi
Opipramol, mental ve fiziksel fonksiyonları etkileyebilir. Bu nedenle, Deprenil tablet tedavisi sırasında araç ve tehlikeli olabilecek makineler kullanılmamalıdır.
YAN ETKİLER/ADVERS ETKİLER
• Tedavinin başlangıcında ortaya çıkan ağız kuruluğu, konstipasyon, akomodasyon güçlüğü, taşikardi, baş dönmesi, palpitasyon, terleme, bulanık görme, miksiyon güçlüğü ilacın periferik ve antikolinerjik etkilerine bağlı olarak ortaya çıkan ve tedaviye devam edilirken ya da tedavinin kesilmesiyle kaybolan etkilerdir.
• Periferik adrenolitik etkisine bağlı olarak ortostatik hipotansiyon, güçsüzlük görülebilir. Bu tür istenmeyen etkilerde genellikle tedavi sürdürülürken ya da tedavinin kesilmesiyle kaybolur.
• Merkezi sinir sistemi üzerindeki etkilerine bağlı olarak somnolans ya da sedasyon sık, titreme, eğilimli hastalarda konvülsiyonlar, geçici mental konfüzyon seyrek olarak görülebilir. Ender olarak, psikomotor fonksiyonların inhibisyonuna bağlı olarak intihar girişimi riskinde artış, mani tarzında kişilik değişiklikleri, deliryum, sinirlilik görülebilir.
• Opipramol tedavisi gören hastalarda kilo artışı meydana gelebilir.
• İlacın yüksek dozları aritmiler, kalp ileti bozuklukları, galaktore, memelerde büyümeye neden olabilir.
• Alerjik deri reaksiyonları, disartri, hepatit, eozinofili, lökopeni, agranülositoz, trombositopeni, impotens ve senkop çok ender olarak görülebilir.
BEKLENMEYEN BİR ETKİ GÖRÜLDÜĞÜNDE DOKTORUNUZA BAŞVURUNUZ.
İLAÇ ETKİLEŞMELERİ VE DİĞER ETKİLEŞMELER
• Opipramol, torsades de pointes türü ventrikül ritim bozukluğu riski nedeniyle sultoprid ile birlikte kullanılmamalıdır.
• Alkol ile birlikte kullanıldığında sedatif etkisinde artış görülür.
• Opipramol, adrenerjik reseptörler üzerinde antagonist etkisiyle klonidin`in hipotansif etkisini inhibe eder.
• Parenteral yoldan uygulanan adrenalin veya noradrenalin ile birlikte kullanılması durumunda hipertansiyon ve ritim bozuklukları görülebilir.
• Antikonvülsan ilaç kullanan hastalarda, opipramol tedavisine başlandığında antikonvülsan dozunun yükseltilmesi gerekebilir.
• Karbamazepin, opipramol`ün karaciğerdeki metabolizmasını arttırır ve konvülsan etkisi nedeniyle generalize konvülsiyon riski artabilir.
• Fluoksetin ve fluvoksamin ile birlikte kullanılması durumunda, plazmadaki antidepresan konsantrasyonları yükselir ve buna bağlı olarak istenmeyen etkilerde artış görülür.
• Baklofen ile birlikte kullanıldığında musküler hipotonik etkide güçlenme görülür.
• Selektif olmayan monoaminoksidaz (MAO) inhibitörleri ile birlikte kullanılması durumunda hipotansiyon ya da hipertansiyon görülebileceğinden, bu tür kombinasyonlardan kaçınılmalıdır.
• Sedatif antihistaminikler, barbitüratlar, hipnotikler, morfin türevleri (analjezik ve antitussif), metadon, nöroleptikler, anksiyolitiklerle birlikte kullanıldıklarında merkezi sinir sistemi üzerindeki depresif etkide güçlenme görülebilir.
• Atropin ve atropin benzeri ilaçlar, Parkinson tedavisinde kullanılan antikolinerjikler, disopramid, fenotiyazinlerle birlikte kullanıldığında, idrar retansiyonu, konstipasyon, ağız kuruluğu gibi istenmeyen etkilerde artış görülebilir.
KULLANMA ŞEKLİ VE DOZU
Deprenil tablet doktor başka şekilde tavsiye etmediği takdirde belirtilen şekilde doz ayarlaması yapılarak oral yolla kullanılır.
Yetişkinlerde yemek ile beraber veya yemekten sonra olmak üzere:
• Hafif vakalarda tercihen akşamları 1-2 tane Deprenil tablet ,
• Orta şiddetli vakalarda, sabah 1 ve akşam 2 tane veya günde 3 defa 1 tane Deprenil tablet
• Şiddetli vakalarda günde 3 defa 2 tane Deprenil tablet kullanılır.
• 6 yaşındaki veya daha büyük çocuklarda opipramol ile ilgili fazla sayıda çalışma yapılmamış olmakla beraber, günlük doz 3-4 mg/kg olarak verilir.
• İlacın etkinliğinin ortaya çıkması için en az 2 hafta süreyle düzenli olarak tedaviye devam edilmiş olmalıdır. Tedaviye 6-8 hafta devam edilmesi önerilir.
• Hekim tavsiyesi ile bu süre daha uzayabilir.
• Yaşlı hastalarda tedaviye mümkün olan en düşük dozlarda başlanmalıdır. Dozun yükseltilmesi gerekiyorsa, bu işlem hastanın gösterdiği toleransa göre yavaş yavaş yapılmalıdır.
• Depresyon tedavisi semptomatiktir. Tedaviye aylarca (6 ay kadar) devam edilmesi, tedavinin kesilmesiyle depresyonun nüksetme riskini engeller.
DOZ AŞIMI VE TEDAVİSİ
Bilinçli ya da bilinçsiz olarak aşırı doz alınması durumunda, ağır kardiyovasküler belirtiler (ileti bozuklukları intoksikasyon belirtisi olarak kabul edilmelidir ), antikolinerjik semptomlar, konfüzyon ve koma görülebilir.
Aşırı doz alan hasta derhal en yakın hastaneye götürülmeli ve tedaviye başlanmalıdır. Doz aşımı durumunda semptomatik tedavi uygulanır ve gereken durumlarda reanimasyon servislerinde solunum ve dolaşım desteği sağlanır.
SAKLAMA KOŞULLARI
Işıktan ve nemden koruyarak, 25ºC`nin altında oda sıcaklığında saklanır.
TİCARİ TAKDİM ŞEKLİ VE AMBALAJ İÇERİĞİ
Deprenil her bir tablette 50 mg opipramol dihidroklorür içeren, 30 tabletlik blister ambalajda piyasaya sunulmuştur.
REÇETE İLE SATILIR
Kaynak: http://www.terrailac.com.tr
